Hallar elementos a partir de los números cuánticos
Ejemplo 1
Si se desea encontrar cuál es el elemento que tiene los siguientes números cuánticos en su último electrón: (4, 2, -1, ½), se debe realizar el siguiente proceso.
Los tres primeros números cuánticos describen el orbital en el que está el electrón: 4d-1
El spin del electrón es ½ y me informa que la flecha va hacia arriba dentro del orbital, es decir, que hasta ahora se están semillenando los orbitales con electrones y que van hasta l igual a -1.
La representación de orbitales o cajas de la capa de valencia del elemento es la siguiente:
Figura 1.
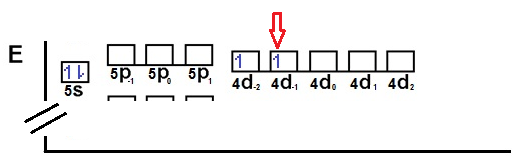
(Para ampliar la imagen haga clic sobre ella)
El elemento desconocido tiene en su capa de valencia el último electrón en el orbital 4d-1 y está señalado con una flecha roja. Los orbitales del nivel o capa de valencia que alojan electrones son todos los que previamente se deben haber llenado, antes del último electrón. Es decir, un electrón en un orbital 4d-2 y los dos electrones del orbital 5s. Recordemos que los orbitales d tienen mayor energía que los s y p y se desplazan a un nivel energético mayor.
En consecuencia, tienen el número cuántico principal disminuido en uno, d(n – 1). El elemento debe tener configuración electrónica de la capa de valencia: 4d25s2 y se encuentra en el periodo 5. El elemento es Zirconio cuya configuración electrónica es [Kr]4d25s2 y configuración de la capa de valencia 4d25s2 tal como la dedujimos.
De aquí en adelante emplearemos para la capa de valencia la siguiente expresión:
ns (n – 2)f (n – 1)d np
Donde n es el nivel energético o periodo, s, p, d y f son los orbitales atómicos de la capa de valencia y si se tienen orbitales d y f toman valores de n – 1 para d y n – 2 para f.
Solo faltaría asignar los electrones a los orbitales de la capa de valencia correspondientes.
Ejemplo 2
Se tiene un elemento con los siguientes números cuánticos en su último electrón (4, 3, -1, -½). Los tres primeros números cuánticos indican que el electrón ocupa el orbital 4f-1. El spin –½ me indica que primero se semillenaron todos los orbitales f con electrones y spin ½, y que ahora se están llenando completamente los orbitales f con electrones y spin – ½ y que el llenado llega hasta el orbital 4f-1. A continuación se representa lo dicho anteriomente.
Figura 2.
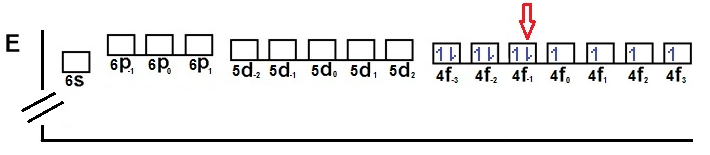
(Para ampliar la imagen haga clic sobre ella)
La flecha roja indica la posición del último electrón para el elemento en cuestión. Los electrones de los orbitales f los escribimos como 4f10. Remplazando en la fórmula de trabajo ns (n – 2)f (n – 1)d np, la configuración de la capa de valencia debe ser 6s24f10, los orbitales d y p se llenan después de los f y por eso no aparecen en esta configuración. El elemento con dicha configuración se encuentra en el periodo 6 (n = 6) y debe pertenecer al bloque f (inmediatamente se explican los bloques en la tabla periódica) en la posición 10. El elemento es Disprosio cuya configuración electrónica es [Xe] 6s24f10 y configuración electrónica de la capa de valencia 6s24f10.
