Introducción
El estado de la materia en el que las partículas se encuentran alejadas unas de otras, con fuerzas casi despreciables de cohesión entre ellas, ocupa todo el volumen del recipiente que los contiene y no tiene forma constante, se define como estado gaseoso.
Las inmensas posibilidades que se presentan para las sustancia hacen de la química una herramienta indispensable en la cotidianeidad y más aún en la áreas de aplicación de las ciencia como el caso de las ingenierías. La industria hace uso intensivo de los aportes de la química para mejorar la calidad y cantidad de productos elaborados.
En el aspecto ambiental se necesario considerar las consecuencias que tienen los procesos y actividades desarrolladas por el hombre sobre su entorno y minimizar el impacto negativo que dichas actividades puedan generar. El aspecto ambiental no es un problema netamente estatal, ya todos contribuimos a generar desechos y podemos aportar, teniendo el conocimiento y las herramientas necesarias.
 |
El ciclo del agua en la tierra genera la circulación de este precioso líquido, vital para la vida y materia prima para muchos procesos industriales. |
Objetivos
Objetivo general
Comprender el comportamiento de los gases y conocer algunas aplicaciones de la química en aspectos industriales y medioambientales.
Objetivos específicos
- Conocer la relación entre las variables de un sistema gaseoso y las implicaciones en su cambio.
- Utilizar el cambio en las variables iníciales para calcular el estado final del sistema.
- Comprender los principios de la electroquímica y sus implicaciones en la corrosión.
- Determinar el pH de una solución y la velocidad de una reacción química.
- Conocer algunas implicaciones ambientales del uso indiscriminado de sustancias químicas.
Gases
Estamos inmersos en una gran masa gaseosa como lo es la atmósfera y de la cual dependemos para vivir. Esta atmósfera ejerce todo el tiempo sobre nosotros una presión a la cual estamos tan acostumbrados que es imperceptible a menos que nos modifiquen estas condiciones.
Las personas que llegan a ciudades elevadas, como la Paz en Bolivia, tienen problemas para respirar normalmente, ya que se reduce la presión exterior haciendo que la cantidad de aire que ingresa a los pulmones sea la misma en volumen, pero contiene una menor cantidad de masa, ya que se reduce la densidad del aire; este problema de respiración se puede ver reflejado en forma favorable para los aviones, pues a medida que vuelan más alto se reduce la densidad del aire y esto disminuye el esfuerzo que se debe realizar para que el aparato avance.
Gases
Características, propiedades, condiciones normales y gases ideales
Los gases cambian su forma y ocupan todo el volumen del recipiente. El cambio de forma requiere tiempo para que ocurra; en caso de que la velocidad de cambio sea demasiado alta se puede llegar a comportar como un sólido, esto se ve reflejado cuando ocurre un evento.
Las denominadas condiciones normales para un gas son las condiciones de una atmósfera de presión y cero grados Celsius (273,15 K) de temperatura.
Los gases idealmente se comportan según la denominada ecuación de los gases ideales:
PV =n RT
P: presión absoluta.
V: volumen.
n: moles de gas.
R: constante universal de los gases ideales.
T: Temperatura de los gases ideales.
Gases
Leyes de Boyle, Charles, Avogadro, Dalton y Graham
El científico británico Robert Boyle (1627-1691) investigó la relación que existía para los gases entre la presión y el volumen descubriendo que a medida que aumenta la presión disminuye el volumen y a medida que se reduce la presión aumenta el volumen, lo que permitió determinar que existe una relación directa entre la presión y el volumen.
El científico francés Jaques Charles (1746-1823), por su parte, observó que para una cantidad de gas constante el volumen se relaciona en forma directa con la temperatura, haciendo que a medida que una de las variables aumenta la otra también lo hace, de igual manera se relacionan cuando hay una disminución. Veamos la siguiente interactividad donde se muestran las relaciones encontradas por estos dos científicos.
La ley de Avogradro enuncia que cuando aumenta la cantidad de materia en un recipiente debe aumentar el volumen del mismo, si se desea conservar en constante la presión. En caso de que el volumen no aumente deberá hacerlo la presión y/o la temperatura hasta contrarrestar el aumento en la cantidad de materia
La ley de Dalton, mientras tanto, enuncia que para una mezcla de gases la presión ejercida sobre las paredes se debe al aporte de todos los componentes de la mezcla.
Finalmente, la ley de Graham establece que para una cantidad idéntica de dos gases a cualquier temperatura sus energías cinéticas son iguales. Si ocurre que uno de los gases posee mayor peso molar significa que sus moléculas se deben mover más lentamente con lo cual es menor la probabilidad que el gas más pesado salga por un pequeño orificio en el recipiente.
Gases
Teoría cinética-molecular
Dentro de esta teoría se deben hacer varias consideraciones que permitan desarrollar el modelo y llegar a conclusiones del comportamiento de los gases que puedan se comparadas con una realidad experimental. Teniendo en cuenta que esta teoría es un modelo de la realidad, se presentan desviaciones entre el modelo y los resultados experimentales que entraran a ser corregidos más adelante mediante valores determinados de forma experimental.
Con base en los postulados, que aparecen en el gráfico de esta pantalla, se establece que si dos partículas con masas diferentes poseen la misma energía cinética, la partícula con menor masa debe tener una mayor velocidad, ya que la relación entre energía cinética y velocidad es:
Ec= ½ mV2
Es de anotar también que es evidente la aproximación de un volumen cero para las partículas del gas.
 |
La teoría debe avanzar en el sentido de poder explicar cada vez mejor la realidad y es hacia ese tipo de modelos que se espera avance la ciencia. El modelo debe cambiar para acercarse a la realidad, ya que la realidad no cambiará para acercarse al modelo. |
Gases
Gases reales y ecuación de Van Der Waals
El comportamiento de los gases no corresponde en su totalidad a lo considerado por la teoría cinética-molecular, y es por ello que se hace necesario llevar a cabo la corrección de la ecuación de los gases ideales mediante coeficientes dependientes de la sustancia considerada.
Las correcciones de la idealidad se ven reflejadas en tablas, gráficas y coeficientes que mejoran la proximidad entre el modelo creado por el hombre y el comportamiento real del sistema.
Actividad de aprendizaje
 |
Resuelve el siguiente crucigrama y fortalece los conocimientos estudiados sobre los gases. |
Aplicaciones de la química a la ingeniería
La aplicación del conocimiento a la solución de situaciones prácticas es lo que define a la ingeniería, y para poder dar solución, se requieren los principios que rigen el comportamiento de la materia, siendo allí donde las ciencias básicas pasan a ser un pilar fundamental.
Aplicaciones de la química a la ingeniería
Materiales de ingeniería
Al considerar los materiales aplicados para cada uso determinado se buscan las propiedades que debe cumplir, estas propiedades son debidas a las interacciones que existen al interior de la sustancia.
La metalurgia es un muy buen ejemplo de la aplicación de la química en la industria ya que los metales se presentan combinados con oxígeno en forma de óxidos. El más común de los procesos es la obtención de hierro con base en materiales ricos en hierro, los cuales se someten a altas temperaturas en las condiciones adecuadas para lograr reducirse a hierro en el alto horno.
C + Fe3O2 -> CO2 + 3Fe
Aplicaciones de la química a la ingeniería
Electroquímica
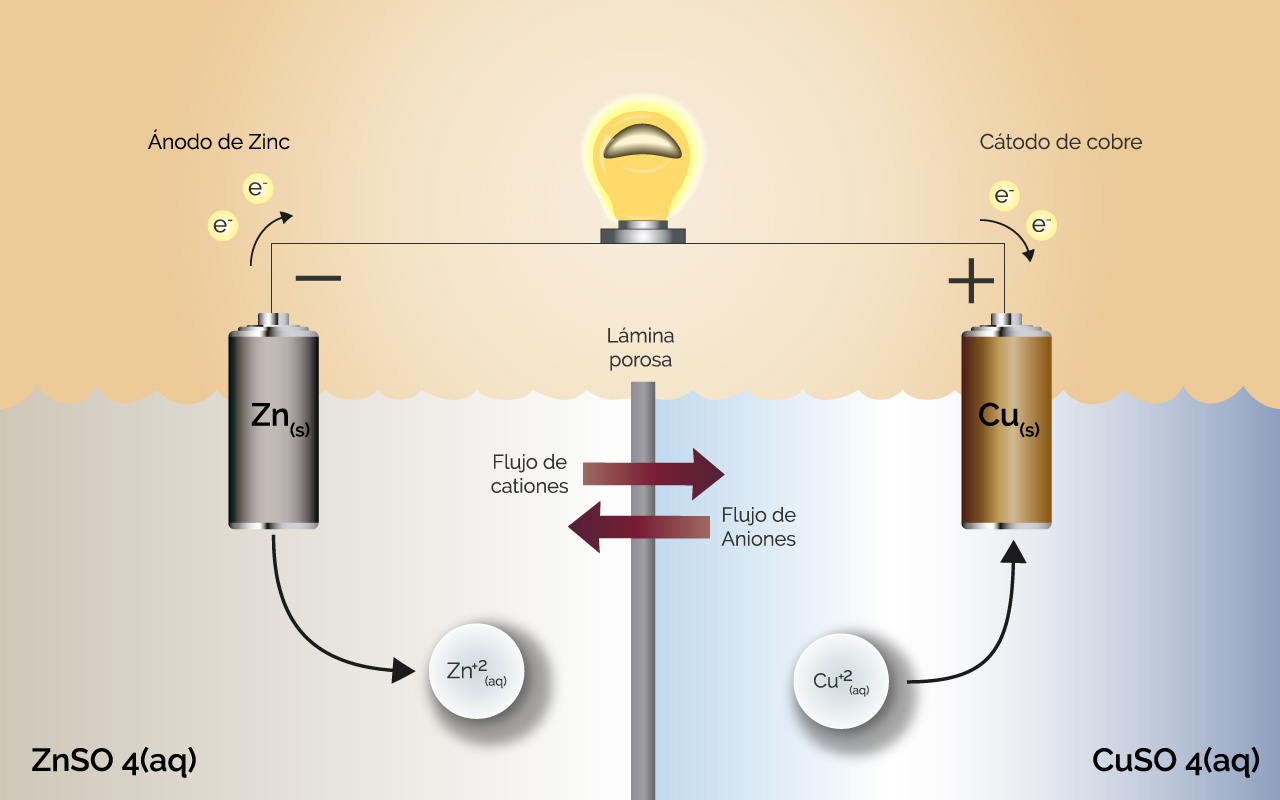
En las reacciones en la que se tiene el cambio de estado de oxidación se presenta el movimiento de electrones en el medio. Este es el principio que rige el funcionamiento de la pilas o baterías, haciendo que el movimiento de estos electrones se realice por fuera del recipiente de reacción.
El lugar donde ocurre la oxidación está separado del lugar donde ocurre la reducción, pero está conectado eléctricamente mediante un puente salino que genera un equilibrio de carga donde ninguno de los compartimientos tiene una carga neta.
Aplicaciones de la química a la ingeniería
pH
Con el fin de determinar la acidez de las soluciones se estableció una medida para la concentración de protones, se define como el logaritmo negativo de la concentración molar de hidronios, que en términos matemáticos es:
pH = -log [H+]
donde [H+] es la concentración molar (moles/L) de iones H+.
Para el caso de las soluciones acuosas el valor se encuentra entre 0 y 14 unidades teniendo el 7 como neutro y los valores menores que 7 como ácidos, mientras que los valores mayores de 7 como básicos. Cuando se desconoce la concentración de H+, pero se conoce la concentración de iones OH- se puede aplicar que:
pH + pOH = 14
Lo anterior se deriva de la constante de disociación del agua puesto que para este solvente puro tiene un valor de 1x10-14.
Aplicaciones de la química a la ingeniería
Cinética química
Las reacciones pueden ser favorecidas en cuanto a que se produzca espontáneamente, pero surge la pregunta de ¿cuál es la velocidad con la que ocurre dicha reacción y cuáles son los factores que la afectan? Para responder la pregunta anterior surge la cinética química, en donde se establece la relación entre la concentración de los reactivos y los productos con la velocidad de cambio.
Por ser consideradas las concentraciones de productos y reactivos se debe tener en cuenta que al inicio de la reacción se tiene la máxima concentración de reactivos y una concentración nula de productos, generando una alta velocidad de conversión y a medida que transcurre el tiempo se consumen reactivos y se generan productos, lo que reduce la velocidad a medida que avanza el tiempo de reacción hasta llegar a un punto en el que la cantidad de reactivos que se consumen para generar productos es igual a la cantidad de reactivos que regresan a su estado original de reactivos, es en el punto final donde se dice haber llegado al equilibrio.
Actividad de aprendizaje
 |
Encuentra todos los términos relevantes sobre la aplicación de la química en la ingeniería. |
Aplicaciones de la química al medio ambiente
Con respecto al tema ambiental, uno de los inconvenientes cuando se investigan y desarrollan proyectos es la imprecisión del término medio ambiente que aparece repetidamente entre líneas pero no se precisa su significado.
Para el propósito de esta unidad, medio ambiente se entenderá como las relaciones e interacciones que se establecen entre los sistemas socioculturales y sus medios ecosistémicos o entornos ampliados.
Cada proceso o transformación química de nivel industrial afecta al medio ambiente. Ejemplos de cambios inducidos en el medio ambiente son la contaminación del aire y el suelo, la pérdida de la capa de ozono, el efecto invernadero y el calentamiento global, la contaminación del agua y los desechos industriales, del petróleo, de la minería, de los procesos de manufactura y producción.
Desde el enfoque de estudio de interacciones, todas estas problemáticas tienen casi que un solo factor generador: el sistema sociocultural y sus dimensiones. Las políticas, leyes y normatividad no son suficientes para evitar la contaminación del agua de los ríos, o los organismos de control no son eficaces o no tienen las herramientas para hacer cumplir la normatividad, o los procesos son tan lentos que una vez que se autorizan ya se han inducidos los cambios, en ocasiones irreversibles. Esto sin nombrar las responsabilidad de las empresas, los ciudadanos o la tecnología empleada.
 |
Un caso como este lo tenemos en el río Bogotá y sus aguas contaminadas de las que no se puede hacer uso, porque contiene una alta carga microbiana, metales pesados como cromo, cadmio, mercurio, plomo, arsénico y cinc, sólidos suspendidos como plásticos, llantas, muebles, colchones, zapatos, prendas de vestir, por mencionar algunos. |
Resumen
La teoría cinética-molecular de los gases y sus implicaciones permite realizar aproximaciones a la realidad. La ecuación de los gases ideales (PV = nRT) es operativa bajo condiciones limitadas, fuera de esas condiciones es necesario aplicar las correcciones que permiten establecer los cambios reales en un sistema gaseoso.
El estudio de los materiales en ingeniería son pilar de los diseños de estructuras y herramientas para realizar las labores.
La determinación cuantitativa del pH es un valor determinante en las reacciones químicas y es por ello que se debe establecer su valor en forma exacta, el pH es el negativo de logaritmo base diez de la concentración molar de protones o hidronios.
Las reacciones químicas tienen una velocidad de ocurrencia que es proporcional a la concentración de los productos e inversamente proporcional a la concentración de los productos.
Bibliografía ()
- Acosta, G. (2010) Manual de Laboratorio de Química General (2da Ed). Bogotá: Universidad Militar Nueva Granada.
- Briceño, C. Y Rodríguez, L. (1993) Química Bogotá: Editorial Educativa, UIS.
- Brown, T. Lemay,H. y Bursten (2009) Química, la ciencia central (11vª Ed) México: Prentice Hall.
- Chang, R. (2010) Química (10ma Ed) México: Ed. Mc Graw-Hill
- Corporación Autónoma Regional de Cundinamarca – CAR (2010) Adecuación hídrica y recuperación ambiental del rio Bogotá. Vol I y II. Bogotá D.C.: Corporación Autónoma Regional de Cundinamarca – CAR.
- Drew, W. (1990). Química general orgánica y biológica. Bogotá, Colombia: McGraw-Hill Latinoamericana S.A.
- Fred, R. (1992) Fundamentos de química. México: Prentice-Hall Hispanoamericana s.a.,
- Hein, M., Arena, S. (2005) Fundamentos de química, (11va Ed) MéxicoD.F.: Thomson Editores, S.A.
- Kotz, J.C. y Treichel, P.M. (2003) Química y reactividad química. (5ta Ed) México D.F.: Thomson.
- MERCK COLOMBIA S.A (1995) El a, b, c, de la seguridad en el laboratorio (3ra Ed). Bogotá, Colombia: Departamento L PRO.
- Mortimer, C. (1985) Química Belmont California. U.S.A: Grupo Editorial Ibero América.
- Peck, L. (1980) Journal of Chemical Education. 57 (517)
- Petrucci, R. (1986) Química General. México: Fondo Educativo Interamericano.
- Routh, J. Eyman, D., Burton, D. (1900) Compendio esencial de química general orgánica y bioquímica. Bogotá, Colombia: Editorial Reverté Colombiana, s.a.
- Rusell, J., Larena, A. (1992) Química General. Bogotá, Colombia: McGraw-Hill Latinoam. S.A.
- Umland, J.B. y Bellama, J.M. (2000) Química General. (3ra Ed) México D.F.: Thomson.
- Vega, J.C. (1992) Química Orgánica para estudiantes de Ingeniería. Santiago: Universidad Católica de Chile
- Whitten, D., Peck, S. (2008) Química (8va Ed) HITTEN, México: Cengage Learning, 2008, Cruz Manca, México
- Wittcott, H., Reuben, B. (1997) Productos químicos orgánicos industriales, I y II, México: Editorial Limusa
Referencias Web
- Quevedo, J. (s.f.) Alfonso Formula (s.f.) Formulación de química inorgánica. [online] Alonsoformula.com.https://www.alonsoformula.com/inorganica/
- ThoughtCo. (s.f.). Famous Chemists and their Achievements. [online]https://www.thoughtco.com/famous-chemists-4133583
- ThoughtCo. (s.f.). Chemistry in Everyday Life. [online]https://www.thoughtco.com/chemistry-in-everyday-life-4133585
- YouTube. (s.f.). SOLOCONOCIMIENTO [online]https://www.youtube.com/user/soloconocimiento
- WebElements. The perodic table of the elements. WebElements.https://www.webelements.com/