Introducción
Estos párrafos abordarán la visión cuantitativa de la ciencia química. Es decir, la medición y el conteo de las propiedades que se trabajen; por ejemplo, la cantidad de sustancia (moles), la energía involucrada en el proceso, las masa de las sustancias iniciales y finales, las relaciones reactivos – productos, entre otras.
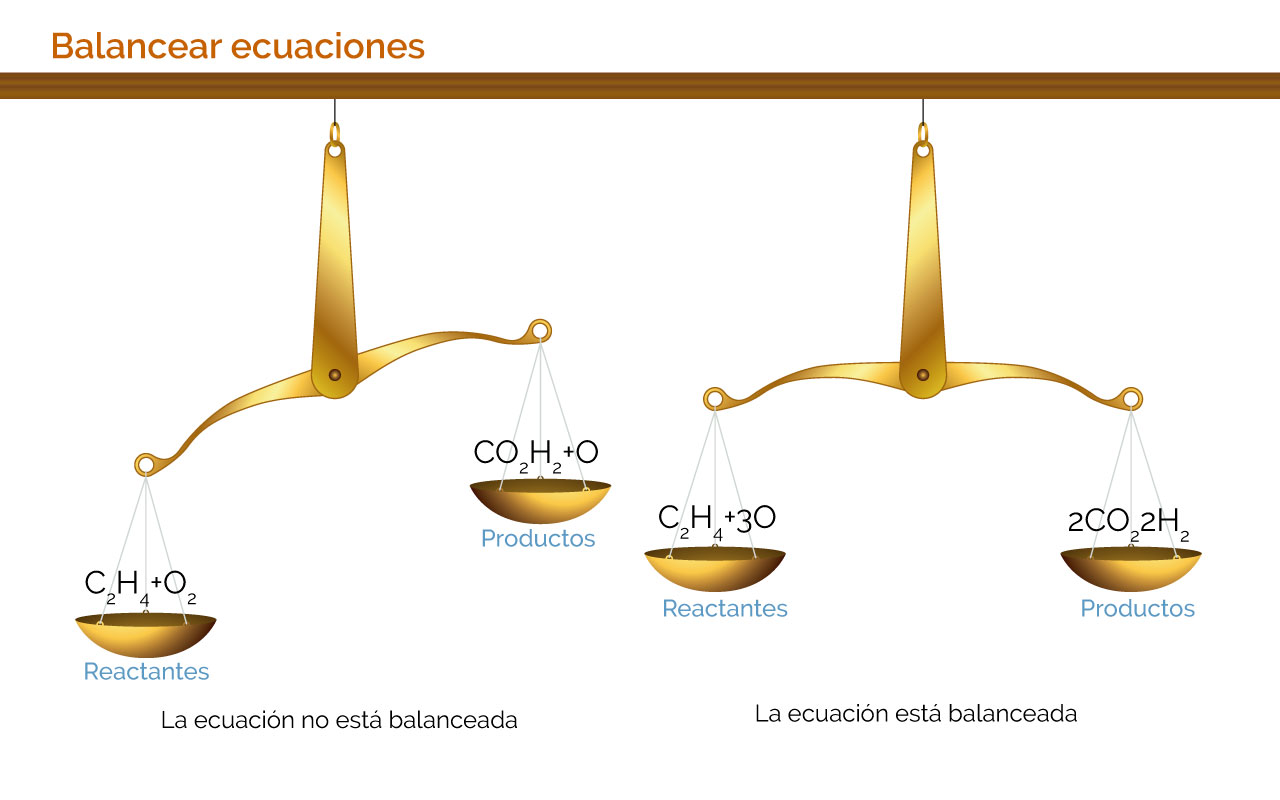
Tal como se trabaja en física y en matemáticas, además de la cuantificación de las propiedades involucradas en los procesos químicos estudiados, existen maneras de balancear y expresar matemáticamente las cantidades de dichas propiedades para el trabajo en química. Todos estos balances son expresados a través de una ecuación, la cual es el punto de partida para la solución de los problemas químicos, ya sean en la industria, la academia, la investigación o el medio ambiente.
Una vez que tenemos completa la ecuación química debemos proceder a relacionar reactivos y productos en moles o unidades de cantidad de sustancia y gramos o cantidad de materia. El abordaje de las relaciones de las sustancias en las reacciones químicas lo hace la estequiometría donde sus cálculos permiten obtener una predicción de cantidades de sustancias en la reacción, rendimientos y purezas de los reactivos. Finalmente se puede extender el estudio estequiométrico de los procesos químicos a las mezclas homogéneas.
Objetivos
Objetivo general
Establecer ecuaciones químicas completas y realizar cálculos estequiométricos con sustancias puras y soluciones donde se conozcan los nombres de los compuestos inorgánicos, a través del estudio de la reactividad de las sustancias químicas, la nomenclatura química y el estudio de las soluciones, con la finalidad de dar bases suficientes para el entendimiento de las transformaciones químicas en la industria, la investigación y el medio ambiente.
Objetivos específicos
- Establecer ecuaciones químicas completas para los procesos químicos.
- Resolver problemas de química que impliquen cálculos estequiométricos.
- Aplicar las reglas de la nomenclatura química para nombrar compuestos inorgánicos.
Tipos de reacciones químicas
Siempre el ser humano se preocupó por entender que le ocurría a la materia cuando él la sometía a distintas condiciones que generaban cambios en sus propiedades y características e incluso cambios de fase. Una vez que pudo relacionar los cambios de las sustancias de partida con las sustancias finales y sus proporciones, obtuvo un enorme cúmulo de datos experimentales y explicaciones de lo ocurrido. Debido al enorme tipo de transformaciones diferentes de la materia, se desarrolló una clasificación por tipos de reacciones para identificarlas rápidamente y poder predecir qué sustancias nuevas o productos se formarían.
Todas las reacciones químicas se pueden representar por medio de una ecuación química. La ecuación química es una forma compacta de presentar una transformación, reacción o cambio químico.
Antes de revisar la clasificación general de las reacciones químicas es importante revisar la solubilidad de los compuestos inorgánicos, ya que ésta determina en muchos casos la posibilidad de que ocurra o no una reacción química.
Tipos de reacciones químicas
Formación de óxidos, hidróxidos, ácidos, bases y sales
Con la información previa sobre la ecuación química y las reglas de solubilidad, se puede comenzar el tema de los tipos de reacción.
Los óxidos son compuestos formados por oxígeno con carga 2- (O2-) y otro elemento que puede ser metálico o no metálico. Los óxidos formados por oxígeno (O2-) y metal se les denomina metálicos o básicos, porque cuando se colocan en agua dan pH básico.
Luego, si a lo anterior se le adiciona agua, obtenemos un hidróxido (OH-) o base, que es un compuesto formado por un metal o ion amonio e hidróxido (OH-) o hidroxilo.
Ahora, los óxidos formados por oxígeno (O2-) y no metal se les denomina ácidos, porque cuando se colocan en agua dan pH ácido. Si además se le adiciona agua al óxido ácido formado, obtenemos un ácido, que es un compuesto formado por hidrógeno (1+), no metal (z+) y oxígeno (2-).
Hasta aquí se ha explicado la formación de óxidos, hidróxidos y ácidos.
Las sales, por su parte, son los compuestos que se forman cuando se reemplazan los hidrógenos 1+ (H+), por metales o ion amonio en los ácidos. Es suficiente con que se remplace un H+ en el ácido para saber que se formó una sal. La reacción en la que se forma una sal a partir de un ácido y una base, se le denomina neutralización. Veamos el siguiente ejemplo.
Tipos de reacciones químicas
Reacciones de desplazamiento simple o sustitución simple
Las reacciones de desplazamiento simple o desplazamiento son reacciones de la forma,
A + BC(ac) AC + B
Donde A es un elemento activo, BC es un compuesto y B es un elemento menos activo que A. Aquí se observa que el elemento A (activo) desplaza a B (menos activo) en su compuesto. Este tipo de reacción se lleva a cabo en solución acuosa. Lo que quiere decir que BC debe ser soluble en agua.
A continuación se analizarán los siguientes casos:
- Metales activos desplazan metales menos activos.
- Metales activos desplazan al H+ de los ácidos no oxidantes.
- Metales activos desplazan al H+ del vapor de agua.
- Metales activos desplazan al H+ del agua líquida.
- No Metales activos desplazan a no metales menos activos.
Tipos de reacciones químicas
Reacción de doble desplazamiento o metátesis
Las reacciones de doble desplazamiento o metátesis son reacciones de la forma,
AB(ac) + CD(ac) AD + CB
Donde AB es un compuesto soluble en agua, CD es un compuesto soluble en agua, AD es un compuesto y CB también. En este tipo de reacciones solo existe un intercambio de iones entre dos compuestos. No existe cambio en el número de oxidación de los elementos ni de carga en los iones. Aquí reaccionan dos compuestos y se forman dos compuestos. Se debe revisar en los compuestos finales la solubilidad. Si entre los iones existe un par que forme un compuesto insoluble, éste se formará.
Se tienen dos tipos de reacciones de doble desplazamiento bien establecidas, pero no son las únicas: Reacciones de precipitación y reacciones ácido – base o de neutralización. En la siguiente ampliación temática se estudiará cada una de ellas.
Tipos de reacciones químicas
Reacciones de reducción–oxidación y oxidación–reducción o redox
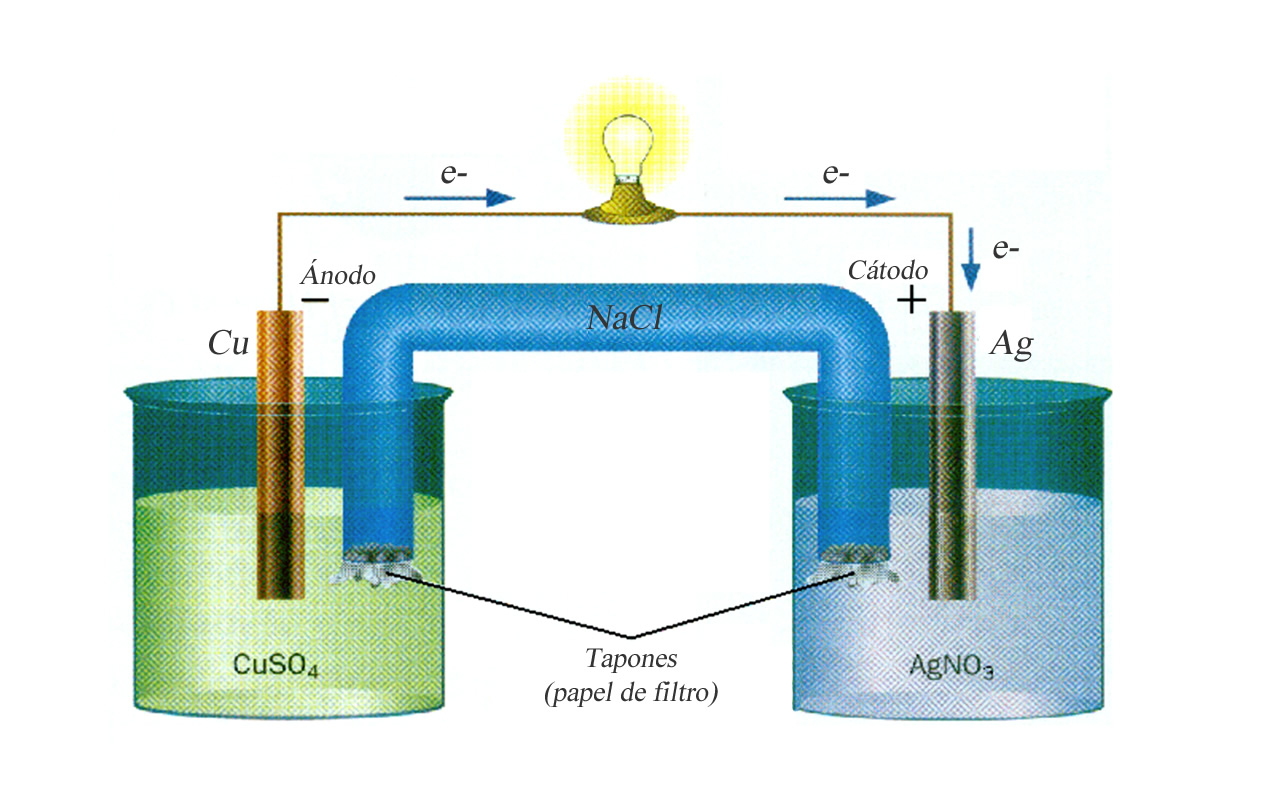
Las reacciones redox son reacciones con transferencia de electrones de un átomo a otro.
Se asignan los números de oxidación a todos los elementos de la ecuación. Si es redox, un átomo (o varios) aumentó su número de oxidación cuando pasó de reactivo a producto. El otro átomo se disminuyó o redujo el número de oxidación cuando pasó de reactivo a producto. A este proceso se le denomina oxidación.
Por lo tanto, un átomo perdió electrones (el que aumentó su número de oxidación) y otro ganó esos electrones (el que disminuyó su número de oxidación) durante la reacción. De esta manera se detecta que una reacción es redox.
Tipos de reacciones químicas
Reacciones de síntesis, combinación o adición
Las reacciones que no clasifiquen como desplazamiento simple, doble desplazamiento o redox, se deben clasificar en otro tipo. Comencemos con las reacciones de síntesis combinación o adición.
Son reacciones de la forma:
A + B →C
Tenemos dos o más reactivos, pero al final un solo producto. Las reacciones de formación de óxidos, hidróxidos y ácidos son de síntesis. Todas las reacciones de síntesis se balancean por tanteo, es decir, elemento por elemento.
Tipos de reacciones químicas
Reacciones de análisis o descomposición
Son reacciones de la forma:
A -> B + C
Todas las reacciones de síntesis se balancean por tanteo, elemento por elemento. Este tipo de reacciones siempre requieren algún tipo de energía.
Existen dos casos en particular, puede ocurrir que reaccione un compuesto para obtener los elementos constituyentes; o puede reaccionar una sal para formar dos o más sustancias, tal como se muestra en el medio de pantalla.
|
Finalmente, es importante de adoptar alguna estrategia para establecer correctamente la ecuación química de un problema o ejercicio. Esta es una estrategia rápida para lograr este cometido:
|
Actividad de aprendizaje
 |
Pon a prueba tus conocimientos sobre las reacciones químicas jugando falso/verdadero. |
Nomenclatura de compuestos inorgánicos
La nomenclatura química es la rama que revisa, estudia y propone maneras sistemáticas y rápidas de dar nombre a los compuestos químicos, de tal manera que no permita ambigüedades en la interpretación de la fórmula química de la sustancia a partir del nombre y viceversa.
De la nomenclatura de uso frecuente se destaca la desarrollada por la (IUPAC) o denominada también nomenclatura STOCK. También existe la nomenclatura tradicional y la sistemática.
En química inorgánica la nomenclatura STOCK es la empleada para óxidos básicos, hidróxidos y compuestos binarios de metales. La nomenclatura sistemática para óxidos ácidos y compuestos binarios de no metales. Para los ácidos y las sales, lo más frecuente es que se utilice la nomenclatura tradicional.
Es decir, debemos conocer las reglas para la nomenclatura de los compuestos inorgánicos, casi desde todos los sistemas de nombres.
Actividad de aprendizaje
 |
Fortalece las normas para nombrar los compuestos inorgánicos completando el siguiente cuadro. |
Estequiometría de las reacciones químicas
La estequiometría es la rama de la química que estudia las relaciones cuantitativas de las sustancias de una reacción. Se cuantifica cantidad de sustancia (moles), cantidad de materia (gramos, kilogramos, libras), cantidad de partículas (moléculas o átomos) y cantidad de energía.
Para comenzar a trabajar la estequiometría de una reacción o problema químico, es necesario tener la ecuación química completa. Luego se organiza la información suministrada, se establecen las cantidades de sustancias en moles y se relacionan en la ecuación química. En la estequiometría la recomendación es trabajar siempre con moles.
Cuando se requiere trabajar con sustancias puras, es posible que en la reacción se tenga una sustancia en mayor cantidad que la requerida. Por lo tanto, se necesita revisar el reactivo limitante y el reactivo en exceso de la reacción. Una vez establecido el reactivo limitante se calcula todo en la reacción con referencia a éste.
No obstante, es necesario realizar los cálculos estequiométricos con sustancias de determinada pureza o que las acompañan impurezas. En estos casos se debe calcular la cantidad de sustancia pura (a partir del porcentaje de pureza) y resolver el problema a partir del reactivo limitante.
Una vez que se calculan las cantidades de las sustancias en el problema, se tienen las cantidades de reactivos consumidos y de productos esperados. A la cantidad esperada de un determinado producto se le denomina rendimiento teórico. A la cantidad de producto obtenido experimentalmente se le denomina rendimiento experimental. El rendimiento de la reacción o porcentaje de rendimiento es el porcentaje que se obtuvo de un producto en una reacción.
 |
Para conocer la eficiencia de una reacción química, se debe hacer lo siguiente: tener el rendimiento reportado en la literatura (rendimiento literatura). El rendimiento realizado del proceso en el laboratorio y compararlo con el de la literatura (rendimiento proceso) y se aplica la siguiente fórmula: Eficiencia del proceso = (rendimiento literatura * rendimiento proceso)/100
|
Mezclas homogéneas y soluciones
Otro punto importante en la resolución de los problemas o planteamientos químicos, es el tratamiento que se le da a las soluciones o mezclas homogéneas. En la naturaleza gran parte de los fenómenos se dan en solución. También en los procesos industriales y de ingeniería, las soluciones juegan un papel central.
Una solución es: una mezcla de dos o más sustancias que retienen sus propiedades y que es homogénea hasta el nivel molecular. Las sustancias (solutos) que se disuelven en el solvente generalmente alcanzan un valor máximo. Este valor se le denomina solubilidad máxima o solubilidad y depende de la temperatura a la que se realice el proceso.
Existen tres tipos de soluciones: insaturada, saturada y sobresauturada. Además de las características de las soluciones, anteriormente expuestas, a veces es necesario prepararlas. Para esto se requiere conocer la concentración de la solución a preparar y luego mezclar soluto y solvente hasta obtener la mezcla homogénea.
Cuando trabajamos reacciones con sustancias en solución, que puede ser acuosa, necesitamos tener en cuenta que se trata de mezclas. En este caso se deben calcular las moles de las sustancias reaccionantes a partir de las concentraciones y luego realizar los cálculos estequiométricos.
Reacción redox avanzada
El siguiente tema trata de las reacciones de reducción – oxidación, oxido – reducción o abreviadamente redox. Gran parte de los fenómenos materiales presentan reacciones redox, es decir reacciones en las que algunos elementos cambian su número o estado de oxidación.
- Plantear las semi – reacciones y balancearlas en masa y carga.
- Igualar el número de electrones en las semi – reacciones y sumarlas (ecuación iónica neta).
- Adicionar las especies espectadoras y revisar balance de carga y masa (ecuación iónica total).
Actividad de aprendizaje
 |
Relaciona los diferentes conceptos esenciales sobre la estequiometría y soluciones, fortaleciendo de esta manera tus conocimientos. |
Resumen
Esta unidad está dedicada a presentar los conceptos y principios de trabajo cuantitativo en química general. Primero se revisan los tipos de reacciones que con más frecuencia se encuentran en los fenómenos naturales y se aprende a reconocerlas y balancearlas.
Segundo, se trabajan las reacciones desde el punto de vista cuantitativo con la estequiometría para sustancias puras, sustancias con impurezas y soluciones.
Por último, Con estas bases los estudiantes están en capacidad de enfrentarse a problemas o ejercicios básicos de química aplicada a la ingeniería, al medio ambiente y la interpretación de los fenómenos químicos en la cotidianidad.
Bibliografía ()
- Acosta, G. (2010) Manual de Laboratorio de Química General (2da Ed). Bogotá: Universidad Militar Nueva Granada.
- Briceño, C. Y Rodríguez, L. (1993) Química Bogotá: Editorial Educativa, UIS.
- Brown, T. Lemay,H. y Bursten (2009) Química, la ciencia central (11vª Ed) México: Prentice Hall.
- Chang, R. (2010) Química (10ma Ed) México: Ed. Mc Graw-Hill
- Corporación Autónoma Regional de Cundinamarca – CAR (2010) Adecuación hídrica y recuperación ambiental del rio Bogotá. Vol I y II. Bogotá D.C.: Corporación Autónoma Regional de Cundinamarca – CAR.
- Drew, W. (1990). Química general orgánica y biológica. Bogotá, Colombia: McGraw-Hill Latinoamericana S.A.
- Fred, R. (1992) Fundamentos de química. México: Prentice-Hall Hispanoamericana s.a.,
- Hein, M., Arena, S. (2005) Fundamentos de química, (11va Ed) MéxicoD.F.: Thomson Editores, S.A.
- Kotz, J.C. y Treichel, P.M. (2003) Química y reactividad química. (5ta Ed) México D.F.: Thomson.
- MERCK COLOMBIA S.A (1995) El a, b, c, de la seguridad en el laboratorio (3ra Ed). Bogotá, Colombia: Departamento L PRO.
- Mortimer, C. (1985) Química Belmont California. U.S.A: Grupo Editorial Ibero América.
- Peck, L. (1980) Journal of Chemical Education. 57 (517)
- Petrucci, R. (1986) Química General. México: Fondo Educativo Interamericano.
- Routh, J. Eyman, D., Burton, D. (1900) Compendio esencial de química general orgánica y bioquímica. Bogotá, Colombia: Editorial Reverté Colombiana, s.a.
- Rusell, J., Larena, A. (1992) Química General. Bogotá, Colombia: McGraw-Hill Latinoam. S.A.
- Umland, J.B. y Bellama, J.M. (2000) Química General. (3ra Ed) México D.F.: Thomson.
- Vega, J.C. (1992) Química Orgánica para estudiantes de Ingeniería. Santiago: Universidad Católica de Chile
- Whitten, D., Peck, S. (2008) Química (8va Ed) HITTEN, México: Cengage Learning, 2008, Cruz Manca, México
- Wittcott, H., Reuben, B. (1997) Productos químicos orgánicos industriales, I y II, México: Editorial Limusa
Referencias Web
- Quevedo, J. (s.f.) Alfonso Formula (s.f.) Formulación de química inorgánica. [online] Alonsoformula.com.https://www.alonsoformula.com/inorganica/
- ThoughtCo. (s.f.). Famous Chemists and their Achievements. [online]https://www.thoughtco.com/famous-chemists-4133583
- ThoughtCo. (s.f.). Chemistry in Everyday Life. [online]https://www.thoughtco.com/chemistry-in-everyday-life-4133585
- YouTube. (s.f.). SOLOCONOCIMIENTO [online]https://www.youtube.com/user/soloconocimiento
- WebElements. The perodic table of the elements. WebElements.https://www.webelements.com/