Introducción
La tendencia de los sistemas a disminuir la energía contenida dentro de ellos lleva a que los constituyentes de un sistema tomen las posiciones y las configuraciones tales que permitan disminuir su energía interna; es así como se crea en la grafica de energía contenida en función del avance de reacción. Es allí donde se puede determinar si una reacción es exergónica o endergónica y también donde se puede observar la energía de activación.
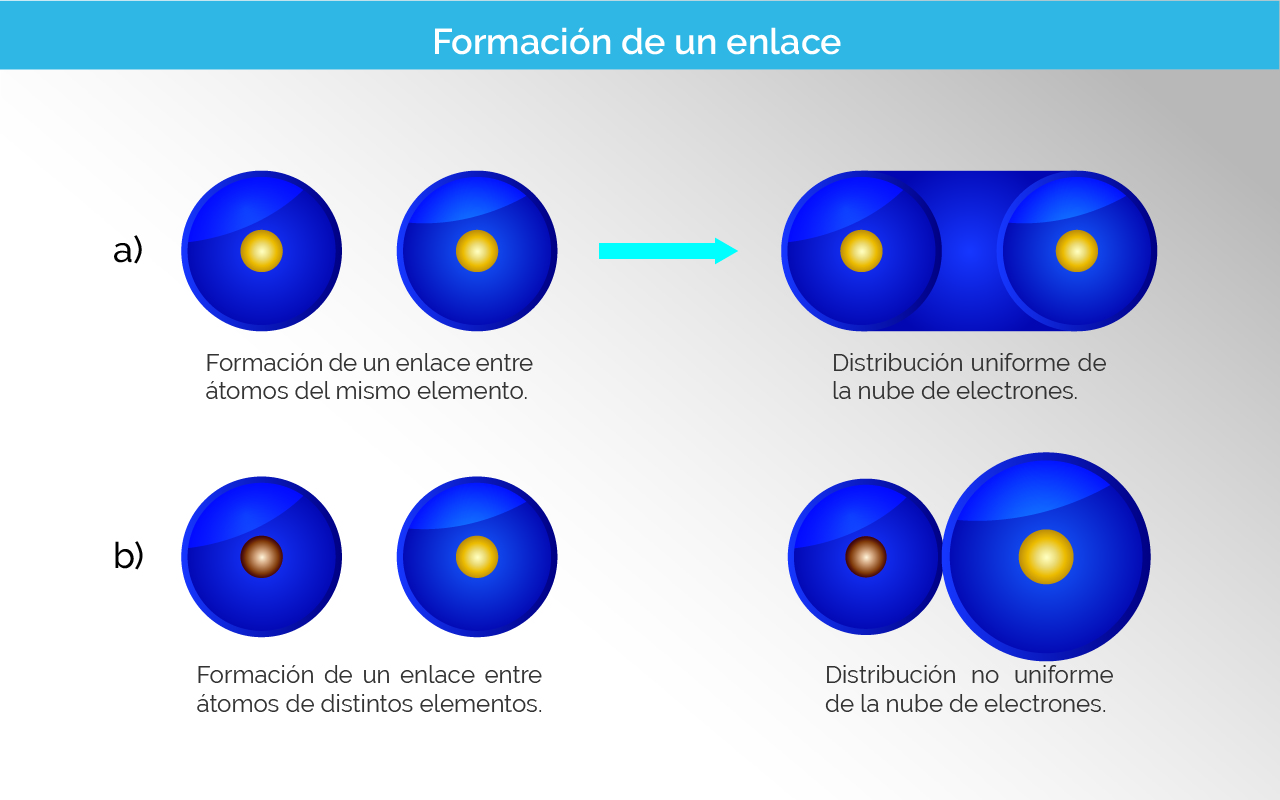
La unión entre átomos para generar moléculas se hace mediante enlaces químicos. La atracción entre cargas opuestas permite establecer una afinidad entre la nube de un átomo y el átomo cercano. Esta atracción tiene una distancia óptima en la cual se tienen las energías de atracción maximizadas y las energías de repulsión, entre cargas iguales, está minimizada. De esta manera, se tiene el diagrama de energía de la distancia interatómica.
Objetivos
Objetivo general
Comprender en forma básica cuáles son las reglas que rigen la formación de moléculas, su estructura y las fuerzas intermoleculares.
Objetivos específicos
- Diagramar los átomos según las estructuras de Lewis .
- Mediante las estructuras de Lewis establecer la estructura plana para las moléculas.
- Determinar la forma tridimensional para la disposición de los enlaces que rodean a un átomo.
- Indicar el tipo de enlace que rige entre dos átomos y la polaridad del mismo.
Polaridad
Recordemos que los electrones tienen carga negativa. Consideremos que existe un átomo neutro que adquirió los electrones que cedió otro átomo. Este que inicialmente tenía una cantidad de protones igual que la cantidad de electrones tiene por ende una descompensación de cargas. En descompensación de cargas significa que las cargas negativas (electrones) es mayor que la cantidad de cargas positivas (protones). Por ello, este átomo que recibe electrones queda con una carga negativa con base a las cargas adoptadas.
Por cada uno de los átomos podemos inferir que el átomo que pierde electrones quedará con carga positiva mientras que el átomo que gana electrones quedará con carga negativa. Cabe decir que no siempre es un átomo el que sede electrones, puede ser uno o más. De igual manera, no solo es un átomo el que debe recibir electrones puede ser uno o más.
Polaridad
Regla del octeto
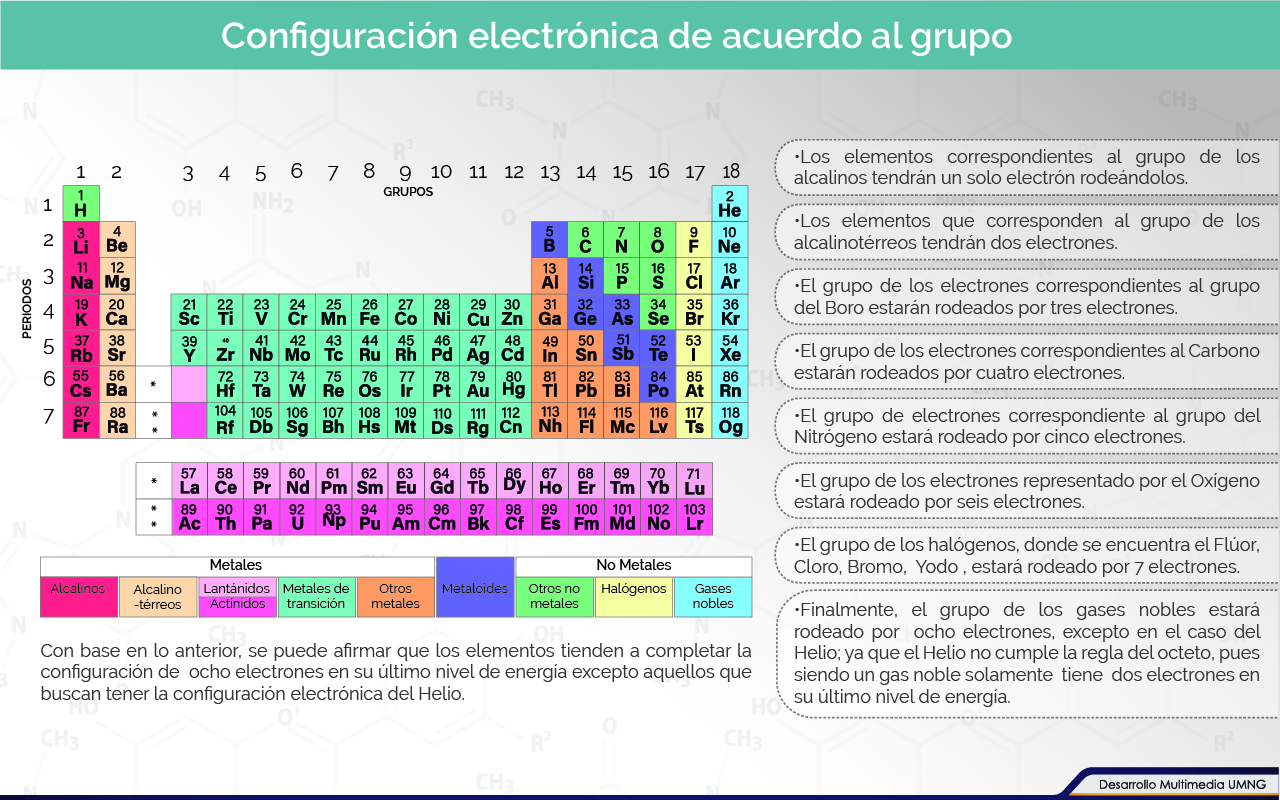
La ley conocida como regla del octeto indica que la configuración electrónica adoptada por cada uno de los átomos participantes en una molécula tiende a semejarse a la configuración electrónica de los gases nobles.
Comúnmente se podría interpretar esto como una tendencia por parte de los átomos y sus creación de enlaces.
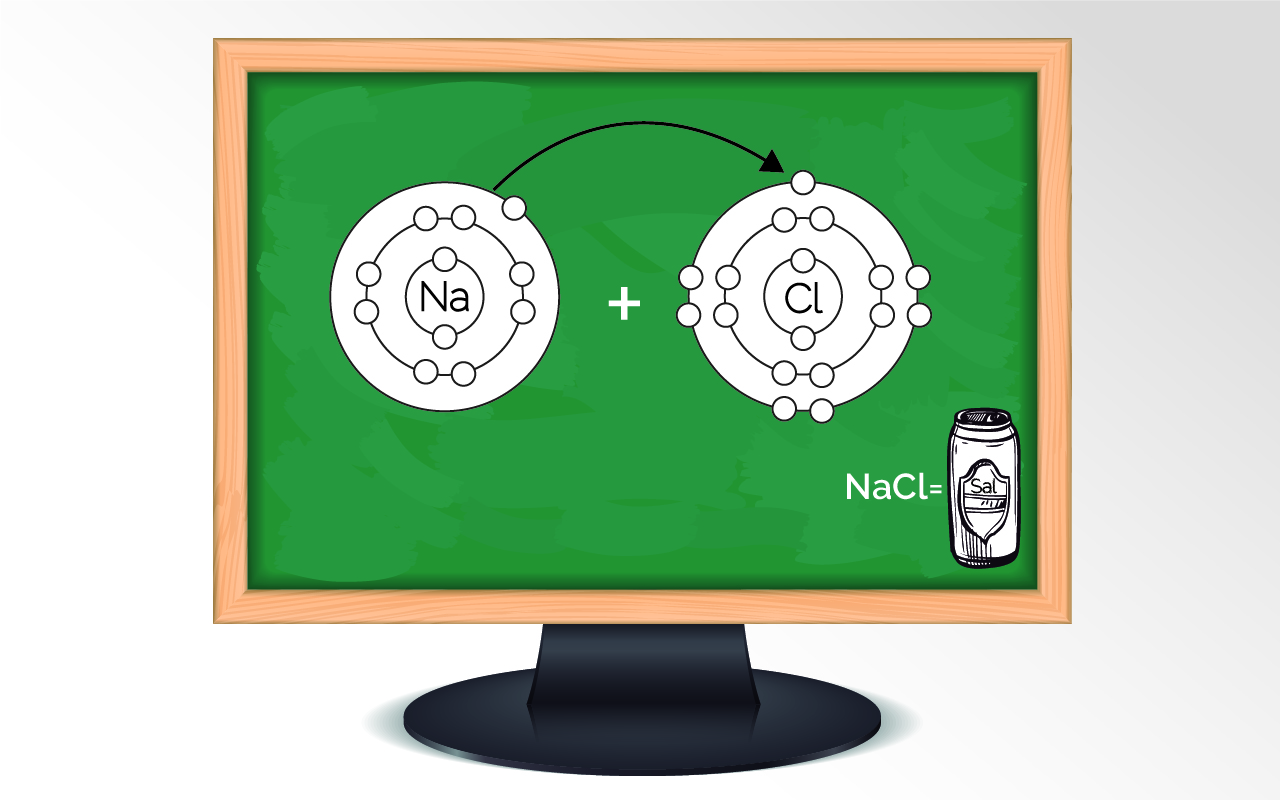
Por ejemplo, se tiene un átomo que desea ceder electrones o perderlos para tomar la configuración del gas noble más cercano.
Si este átomo está perdiendo electrones debe existir un átomo tal que los reciba, planteando que el primero inicialmente se encontraba en forma neutra. Es decir, que la cantidad de protones es igual a la cantidad de electrones. Entonces se debe considerar que el número de cargas positivas en el núcleo será mayor que el número de cargas en la periferias.
La suma de carga o el balance neto de carga para este átomo quedará descompensado ya que la cantidad de protones en el núcleo es tal que aparte de neutralizar la cantidad de electrones en la periferia da una carga positiva a todo el átomo.
 |
Para un mejor entendimiento se recomienda ver el siguiente ejemplo. |
Polaridad
Enlace iónico, covalente y metálico
Un enlace químico corresponde a la fuerza que une o enlaza a dos átomos, sean estos iguales o distintos, de una molécula. La unión de estos busca alcanzar la estabilidad al tratar de parecerse al gas noble más cercano, como se dijo anteriormente. Los enlaces son el resultado de los movimientos de los electrones del último nivel energético o electrones de valencia.
Los enlaces se pueden clasificar en tres grupos:
- Enlaces iónicos.
- Enlaces covalentes.
- Enlaces metálicos.
Moléculas
La unión de dos o más átomos mediante enlaces químicos da lugar a la formación de una molécula, sin importar que los átomos que la constituyen sean del mismo elemento.
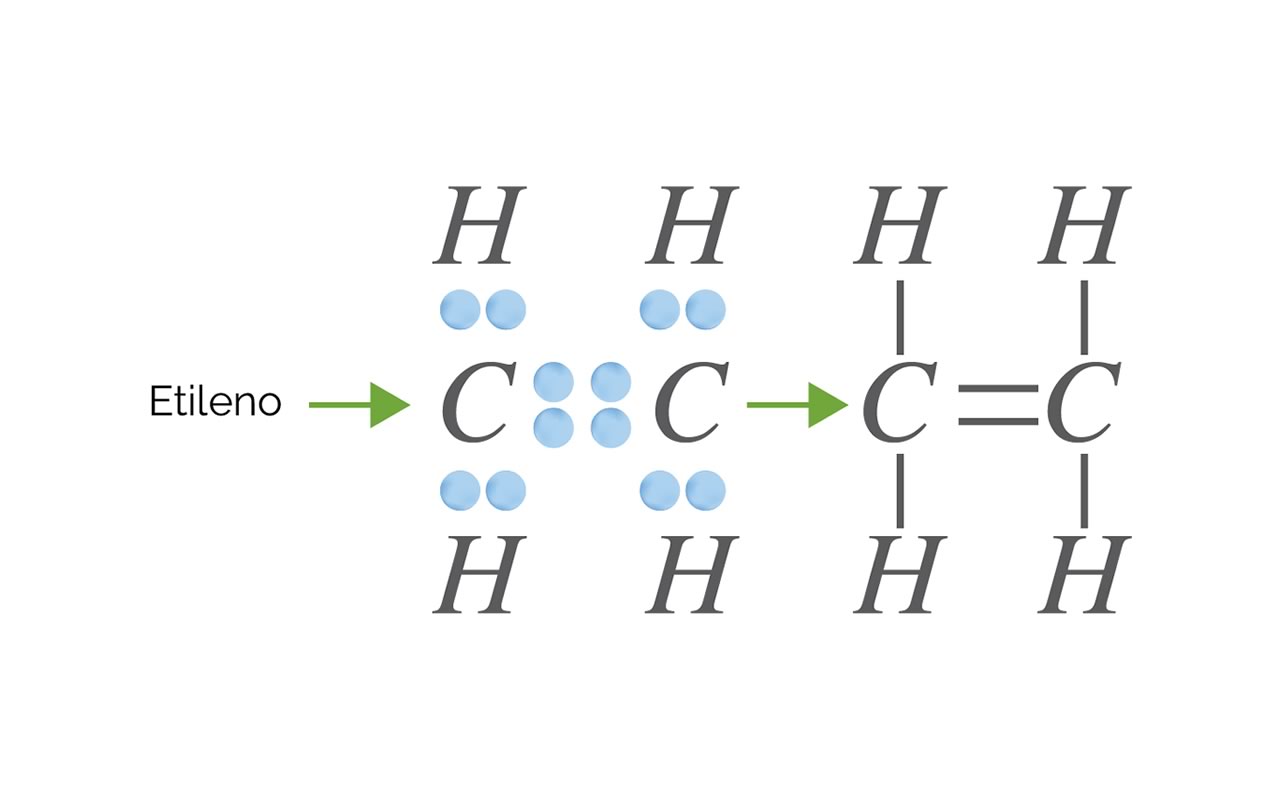
Es así como podemos hablar de molécula cuando se unen dos átomos de oxigeno para que mediante enlace covalente doble se forme una molécula de oxigeno (O2).
Moléculas
Fuerzas intermoleculares
Son aquellas que se presentan entre moléculas diferentes sin que este tipo de interacciones tengan la energía suficiente para ser considerada un enlace. Por lo tanto, se puede inferir que es más fácil contrarrestar energías intermoleculares que contrarrestar enlaces.
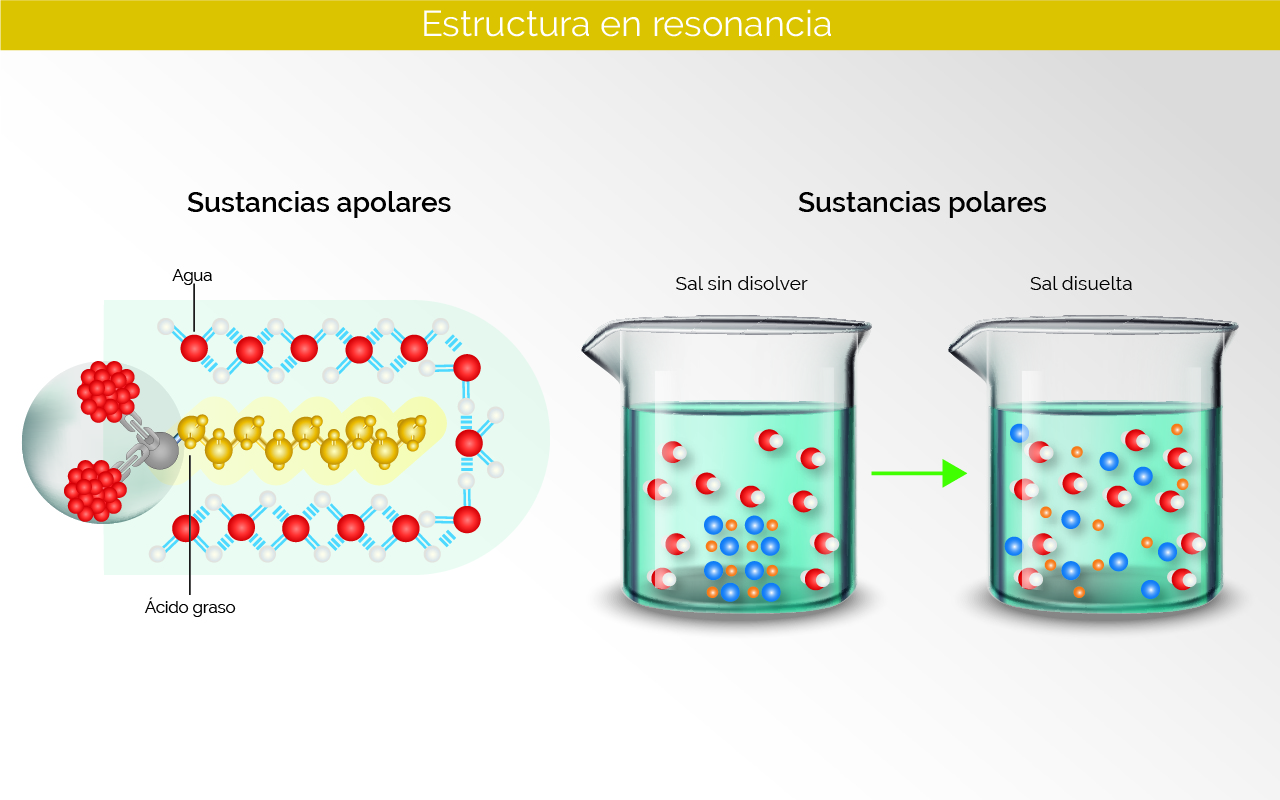
Las interacciones moleculares nos permiten determinar qué moléculas polares tienden a interactuar con moléculas que también tienen una descompensación de carga entre sus constituyentes. Esto quiere decir que moléculas polares son atraídas por otras moléculas polares y en el caso contrario, es decir que la molécula no tenga una polaridad alta ella se verá atraída por parte de moléculas que tienen también una baja polaridad. Por ello las interacciones moleculares son determinantes para saber si una sustancia es o no es soluble en otra sustancia.
Cuando se crean soluciones, el soluto debe tener afinidad por el solvente. Esta afinidad es creada por la polaridad. Entonces se puede decir que solutos polares se disuelven en solventes polares.
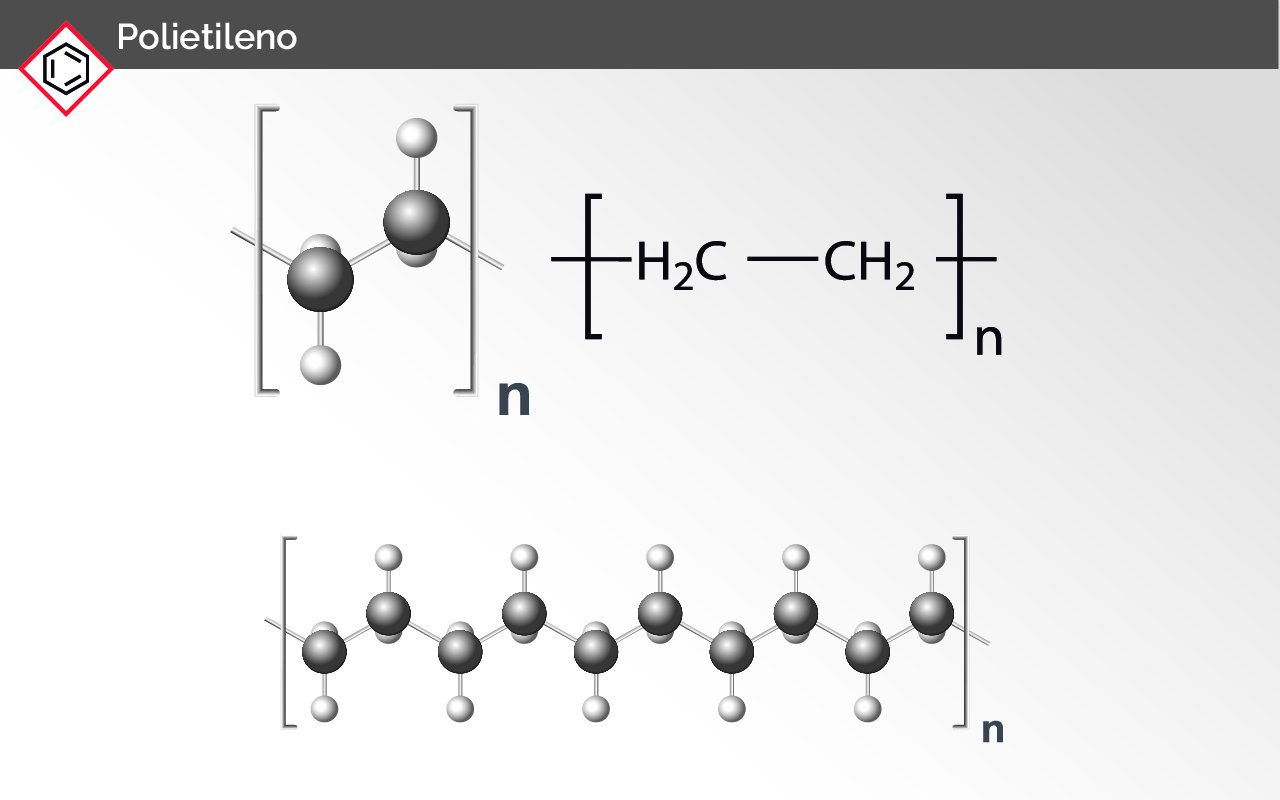
En el caso de las sustancias poco polares, como lo son aquellas sustancias constituidas únicamente por carbono e hidrógeno, es decir hidrocarburos, son sustancias que tienen baja solubilidad.
Moléculas
Estructuras de Lewis
El químico estadounidense G.N. Lewis (1875-1946) sugirió una forma sencilla para representar los enlaces basados en los electrones de valencia. Los enlaces externos serán considerados aquellos que no son parte de la estructura electrónica de un gas noble. En la tabla periódica la representación para la configuración electrónica de algunos de los elementos, en su gran mayoría aquellos con alto peso molecular, es representada como la configuración electrónica del gas noble anterior mas una cantidad de electrones adicionales. En la estructura de Lewis, son estos electrones adicionales aquellos que serán considerados para su diagramación.
La representación de la estructura de Lewis consiste en el símbolo del elemento rodeado por los electrones, los cuales se encuentran en cuatro lados específicos: arriba, abajo, izquierda, derecha. En cada uno de estos lugares caben dos electrones. Para mayor claridad se recomienda ver el siguiente ejemplo del azufre.
Para dibujar estructuras de Lewis debemos tener ciertos parámetros. Para determinar la estructura de una molécula constituida por átomos lo primero que se debe hacer es determinar la cantidad total de electrones de valencia. Es decir sumar los electrones de valencia de cada uno de los átomos participantes en la molécula. De esta forma se conoce también la cantidad de electrones que hacen falta para completar la ley del octeto.
Una vez que se conoce la cantidad de electrones y enlaces que se deben formar en la molécula colocamos el átomo central, el cual tiene la menor electronegatividad, y a él sele hacen las uniones. Analicemos el siguiente ejemplo: tricloruro de fósforo.
 |
Recuerde que el Hidrógeno debe formar un solo enlace covalente porque él quiere completar dos electrones en su última capa y no ocho como normalmente se podría llegar a considerar. |
Moléculas
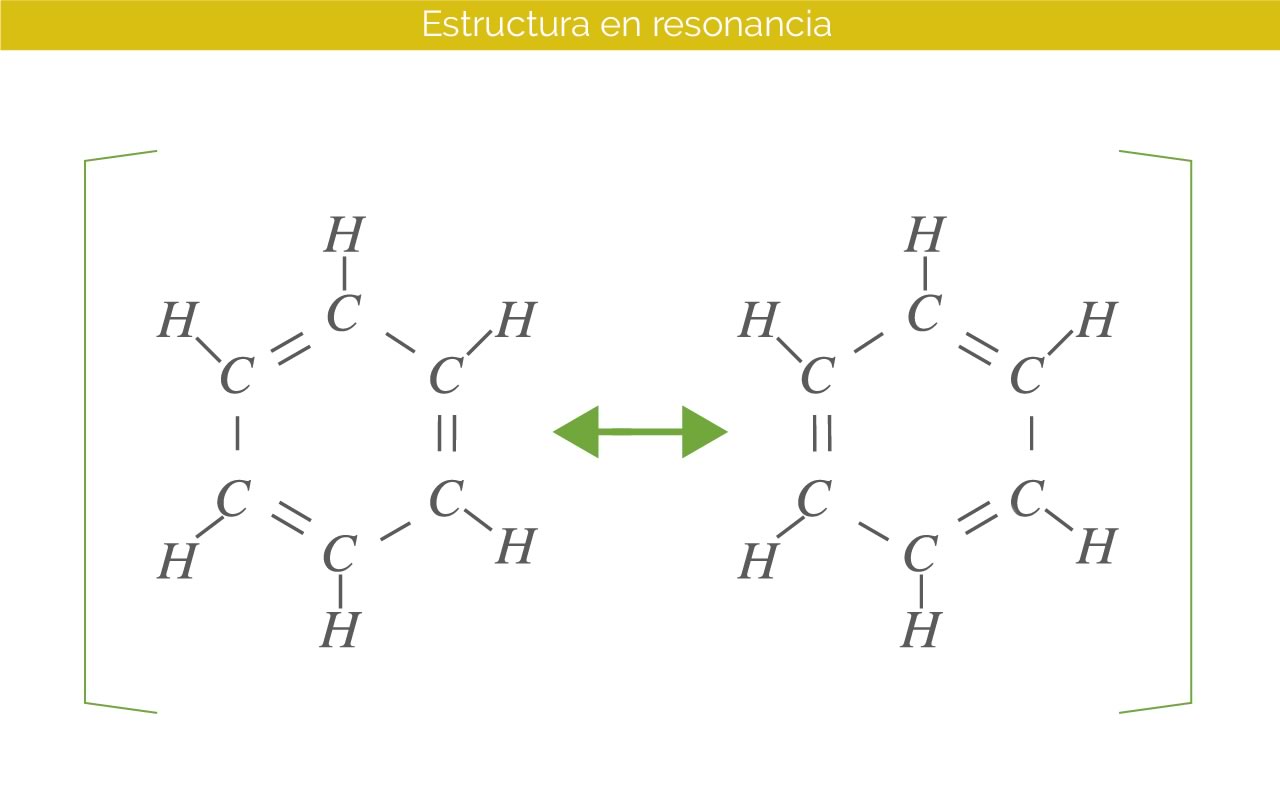
Estructuras resonantes
Cuando se presentan diferentes formas en las cuales se puede dar la configuración para una misma molécula decimos que existen diferentes estructuras para esa molécula. Cada una de esas tendrá un tiempo de estabilidad, permitiendo un mayor aporte a la estructura real de la molécula. Las diferentes estructuras o configuraciones, en las cuales puede estar una molécula, son conocidas como estructuras resonantes; a medida que aumenta la cantidad de estructuras resonantes, la molécula gana estabilidad.
Las estructuras de Lewis son útiles para visualizar las moléculas en dos dimensiones, pero las moléculas reales existen en tres dimensiones por ende debemos tener la posibilidad de pasar de estructuras bidimensionales a tridimensionales.
Esta posibilidad no la brinda el principio de repulsión entre cargas de igual signo. Pues como es sabido, los electrones tienen carga negativa y aquellos que se encuentran en pareja están unidos gracias a su diferencia en su espín.
Cuando una pareja de electrones se acerca a otra pareja de electrones entre estas dos parejas se produce una repulsión por carga y se ubican en las posiciones más alejadas posible.
Moléculas
Estructura molecular
Cuando se representa en un plano las moléculas se tiene el defecto de hacer caso omiso de la tercera dimensión que tiene el espacio. Debido a lo anterior podemos preguntarnos ¿cómo son realmente las moléculas?
Si consideramos que tenemos un átomo rodeado por dos pares de electrones únicamente sabemos que la posición más alejada entre éstos será de ciento ochenta grados, uno opuesto totalmente al otro. Si estos pares electrónicos están participando en enlaces, los enlaces formarán ángulo de ciento ochenta grados por lo que se ubicarán en los extremos del átomo central. Ejemplos de lo anterior están el dióxido de carbono y el amoniaco.
Actividad de aprendizaje
 |
Relaciona los conceptos fundamentales vistos en esta unidad y conoce cuánto haz aprendido. |
Resumen
La formación de moléculas mediante enlaces se debe a la tendencia de los sistemas para reducir su energía. Las moléculas se forman mediante enlaces que pueden ser iónicos, covalente o metálicos. Al formarse la molécula se puede generar una desigualdad en la distribución de los electrones generando carga neta o parcial sobre los átomos; este grado de carga a medida que aumenta el punto de ebullición, establece la solubilidad. De ahí que lo polar sea soluble en polar y lo apolar es soluble en lo apolar.
Con el fin de determinar la forma en la que está estructurada una molécula, se toma como referencia la estructura de Lewis; considerando únicamente los electrones del último nivel de energía para cada elemento y buscando la estabilidad de todos los que componen la molécula. La estabilidad se alcanza cuando todos llegan a la configuración electrónica de un gas noble.
Estructuralmente se considera que tridimensionalmente la orientación de los enlaces se basa en la repulsión que existe entre cada par electrónico.
Bibliografía ()
- Acosta, G. (2010) Manual de Laboratorio de Química General (2da Ed). Bogotá: Universidad Militar Nueva Granada.
- Briceño, C. Y Rodríguez, L. (1993) Química Bogotá: Editorial Educativa, UIS.
- Brown, T. Lemay,H. y Bursten (2009) Química, la ciencia central (11vª Ed) México: Prentice Hall.
- Chang, R. (2010) Química (10ma Ed) México: Ed. Mc Graw-Hill
- Corporación Autónoma Regional de Cundinamarca – CAR (2010) Adecuación hídrica y recuperación ambiental del rio Bogotá. Vol I y II. Bogotá D.C.: Corporación Autónoma Regional de Cundinamarca – CAR.
- Drew, W. (1990). Química general orgánica y biológica. Bogotá, Colombia: McGraw-Hill Latinoamericana S.A.
- Fred, R. (1992) Fundamentos de química. México: Prentice-Hall Hispanoamericana s.a.,
- Hein, M., Arena, S. (2005) Fundamentos de química, (11va Ed) MéxicoD.F.: Thomson Editores, S.A.
- Kotz, J.C. y Treichel, P.M. (2003) Química y reactividad química. (5ta Ed) México D.F.: Thomson.
- MERCK COLOMBIA S.A (1995) El a, b, c, de la seguridad en el laboratorio (3ra Ed). Bogotá, Colombia: Departamento L PRO.
- Mortimer, C. (1985) Química Belmont California. U.S.A: Grupo Editorial Ibero América.
- Peck, L. (1980) Journal of Chemical Education. 57 (517)
- Petrucci, R. (1986) Química General. México: Fondo Educativo Interamericano.
- Routh, J. Eyman, D., Burton, D. (1900) Compendio esencial de química general orgánica y bioquímica. Bogotá, Colombia: Editorial Reverté Colombiana, s.a.
- Rusell, J., Larena, A. (1992) Química General. Bogotá, Colombia: McGraw-Hill Latinoam. S.A.
- Umland, J.B. y Bellama, J.M. (2000) Química General. (3ra Ed) México D.F.: Thomson.
- Vega, J.C. (1992) Química Orgánica para estudiantes de Ingeniería. Santiago: Universidad Católica de Chile
- Whitten, D., Peck, S. (2008) Química (8va Ed) HITTEN, México: Cengage Learning, 2008, Cruz Manca, México
- Wittcott, H., Reuben, B. (1997) Productos químicos orgánicos industriales, I y II, México: Editorial Limusa
Referencias Web
- Quevedo, J. (s.f.) Alfonso Formula (s.f.) Formulación de química inorgánica. [online] Alonsoformula.com.https://www.alonsoformula.com/inorganica/
- ThoughtCo. (s.f.). Famous Chemists and their Achievements. [online]https://www.thoughtco.com/famous-chemists-4133583
- ThoughtCo. (s.f.). Chemistry in Everyday Life. [online]https://www.thoughtco.com/chemistry-in-everyday-life-4133585
- YouTube. (s.f.). SOLOCONOCIMIENTO [online]https://www.youtube.com/user/soloconocimiento
- WebElements. The perodic table of the elements. WebElements.https://www.webelements.com/