Introducción
El ser humano ha recorrido un camino para conocer y reconocer su entorno. Se ha preguntado por las características y el comportamiento del mismo. También se ha enfocado en la revisión de su constitución, es decir la revisión de los constituyentes mínimos tanto materiales como energéticos de todo lo que lo rodea.
Como resultado de esta tarea monumental, fueron desarrollados modelos de los constituyentes primarios de la materia, los átomos, que permiten explicar y predecir el comportamiento de los fenómenos materiales y sus transformaciones.
A partir de las propiedades de los elementos (que se encuentran constituidos por miles de triillones de átomos), se halló cierta regularidad en esas propiedades. Cada cierto valor de número atómico vuelven a repetirse las propiedades ya observadas. El arreglo final de la tabla periódica que conocemos en la actualidad fue desarrollado por el químico ruso Dmitri Mendeléiev.
Entonces, resultado del ordenamiento de los elementos en la tabla periódica, se han reconocido las propiedades periódicas de los mismos, que facilitan entender el comportamiento químico de los elementos y sus características generales.
Objetivos
Objetivo general
Reconocer las propiedades periódicas de los elementos, su organización en la tabla periódica y la existencia de los átomos, su estructura y características. Dicho reconocimiento se realizará a través del estudio de las principales teorías y desarrollos de la química y física de los átomos, con el fin de dar bases suficientes para el entendimiento de la formación de los enlaces químicos, la estructura química y la reactividad química.
Objetivos específicos
- Reconocer la estructura de los átomos y su configuración electrónica.
- Reconocer las implicaciones de la estructura atómica y la configuración electrónica en las propiedades periódicas.
- Identificar las propiedades periódicas de los elementos y sus implicaciones en la formación de iones y enlaces.
El átomo
El objetivo principal de este tema es presentar de manera concreta las ideas y principales conocimientos sobre la estructura de los átomos, desde el punto de vista químico. Es decir, desde los electrones, protones y neutrones y su arreglo en los átomos.
La idea de un atomismo de la sustancia, como idea filosófica o metafísica de la constitución de la materia, fue declarada inicialmente por Leucipo, Demócrito y los epicúreos, quienes atribuían a los átomos las notas del ser único de Parménides de Elea, con lo que reducían la cualidad a la cantidad.
En otras palabras, ellos sostenían que existían constituyentes mínimos e individuales de los fenómenos materiales, denominados átomos, que constituían a todo ser. Incluso en la filosofía medieval se conservó la doctrina corpuscular por los alquimistas y algunos filósofos como Guillermo de Conches.
Durante el renacimiento hubo pensadores como Nicolás de Cusa, Jordano Bruno o Descartes y su teoría de la luz, que impulsaron las ideas atomistas, con aparente desplazamiento del aristotelismo como doctrina filosófica.
Durante esta época surgieron corrientes antiaristotélicas en favor de varias corrientes de pensamiento atomista, (ver el gráfico anterior). Desde este momento, se establecieron los principios para una teoría atómica de los fenómenos materiales, base de la química moderna.
 |
El descubrimiento de la estructura atómica tomó varias décadas. Desentrañar la estructura de los constituyentes de la materia fue una tarea ardua y laboriosa. Finalmente los científicos hallaron maneras de estudiar esas partículas diminutas y esclarecer su distribución interna, tal como se muestra en el anterior video. |
El Átomo
Estructura atómica
Una vez formulados los principios científicos que sustentaban la existencia de los átomos, los investigadores comenzaron a indagar sobre las características de dichos átomos. Veamos cómo fue el desarrollo.
A partir de los experimentos de la estructura de los átomos, se determinó que:
- El número de protones en el núcleo atómico da la identidad del átomo o elemento.
- Los neutrones son partículas necesarias para darle estabilidad al núcleo.
- Los electrones son los encargados de formar los enlaces químicos.
El Átomo
Teoría cuántica
Una vez establecida la estructura de los átomos, la investigación química de los fenómenos materiales se orientó al estudio de las maneras como se enlazaban éstos en las moléculas. A pesar del conocimiento amplio sobre las combinaciones entre elementos para formar compuestos, no se conocía cómo se establecían dichas combinaciones a nivel atómico.
La manera de resolver esta falta de conocimiento partió de las estructura de los átomos, específicamente de la distribución energética de sus electrones, donde se desarrollaron varios modelos. Los más destacados son el modelo planetario de Bohr y el de Sommerfeld.
Pero existían algunas inconsistencias con dichos modelos. Esto ocasionó que los investigadores fueran escépticos para adoptar el modelo planetario de manera válida para la explicación de la organización de los electrones en los átomos.
Mientras tanto los físicos investigaban las anomalías que presentaba la física clásica para la explicación de la estructura atómica y la formación de las moléculas y ajustaban sus modelos a los resultados experimentales. Esta nueva rama de la física se conoce como física cuántica o mecánica cuántica.
Brevemente se pueden describir los principios de trabajo de la mecánica cuántica para los sistemas atómicos y moleculares en la siguiente interactividad.
El Átomo
Números cuánticos
A partir de los resultados mecánico – cuánticos para los átomos, constituyentes de los elementos, se halló que la caracterización energética de los electrones se puede establecer con un conjunto de reglas aplicadas a ciertos valores obtenidos de los números cuánticos.
Los números cuánticos son cuatro, n, l, ml y ms. Cada uno indica una característica energética del electrón en el átomo.
El número cuántico principal o nivel n, indica el nivel de energía que ocupa el electrón en el átomo. Número cuántico azimutal l o subnivel indica el subnivel dentro del nivel energético que ocupa el electrón y depende de n. Los números cuánticos ml y ms, representan la orientación de la región energética y el valor del spin o giro del electrón, respectivamente.
El orbital atómico describe la densidad de probabilidad de carga negativa dentro del átomo debido a los electrones. Cualquier orbital atómico se describe por el nivel energético n en el que se encuentra, el subnivel l y la orientación en un eje coordenado ml y es capaz de alojar 2 electrones.
Es decir, un orbital atómico es un subnivel energético orientado que se encuentra en un nivel de energía determinado dentro del átomo y que puede alojar máximo 2 electrones.
El Átomo
Configuración electrónica
Con los valores de los números cuánticos para la caracterización de los electrones, que se encuentran en un átomo, podemos realizar una descripción del ordenamiento energético de los mismos a un elemento. Esto se conoce como configuración electrónica, distribución electrónica o estructura electrónica.
El ordenamiento energético de los orbitales atómicos no cambia. Los electrones ocupan los orbitales desde el de menor energía, 1s, hasta asignar un orbital al último electrón del elemento. Esta regla se conoce como el principio de construcción o de aufbau.
El número atómico de un elemento en la tabla periódica indica el número de protones, pero también de electrones de sus átomos constituyentes en su estado de menor energía o fundamental. A dichos átomos no se les adicionó ni retiró electrones y tampoco los electrones se encuentran en niveles mayores de energía. Veamos el ejemplo del hidrógeno.
Los demás elementos químicos tienen su configuración electrónica determinada, que establece sus posibilidades de formación de enlaces. En general, los electrones de cualquier átomo tienen distintos números cuánticos. Este enunciado se conoce como el principio de exclusión de Pauli. Ningún átomo tiene dos electrones con idénticos números cuánticos, por lo menos difieren en uno.
Otra manera de emplear los números cuánticos de los electrones es para hallar elementos desconocidos.
 |
De acuerdo con lo anterior, se puede representar la configuración electrónica de cualquier elemento en diagrama de cajas o celdas. Lo importante es comprender cómo se construye el diagrama, ya que la configuración electrónica se encuentra en la tabla periódica. Se recomienda adquirir siempre una buena tabla periódica. |
Actividad de aprendizaje
 |
Resuelve el siguiente crucigrama con base en todo lo visto hasta este punto sobre el átomo. |
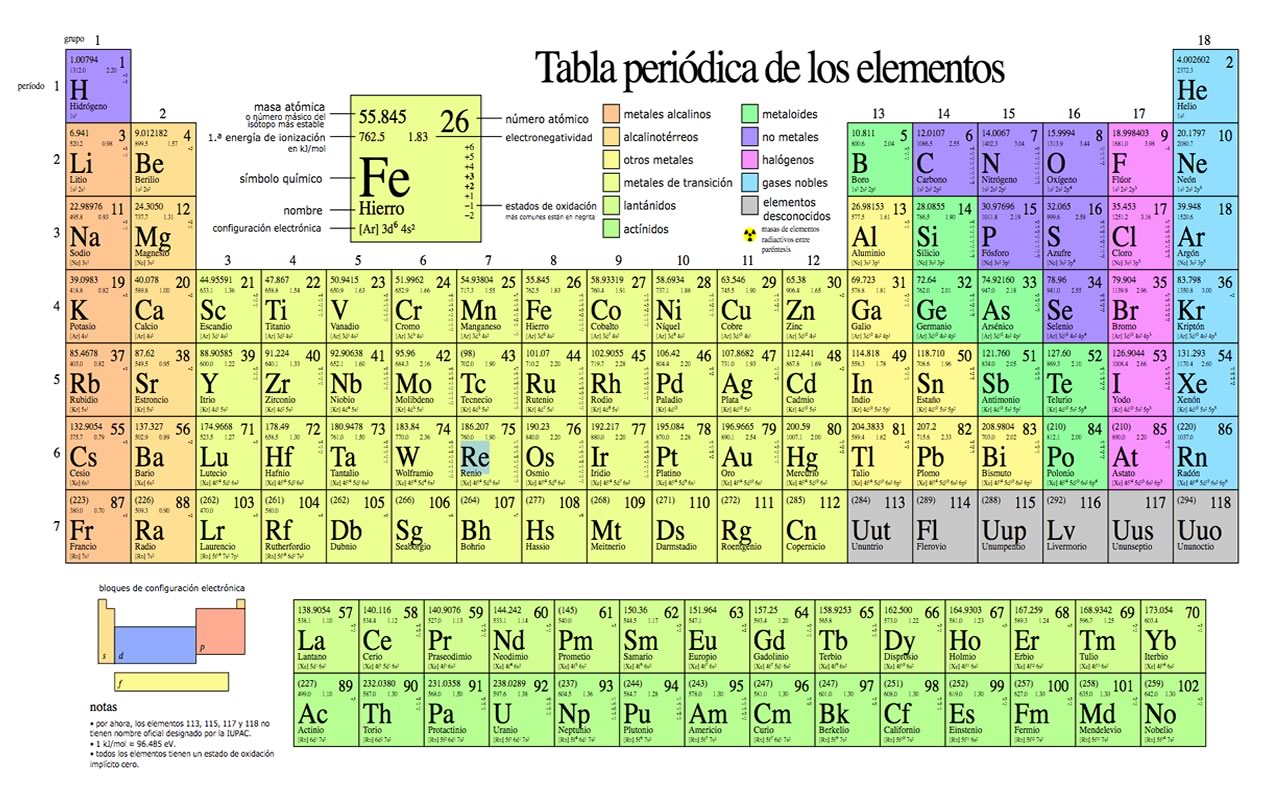
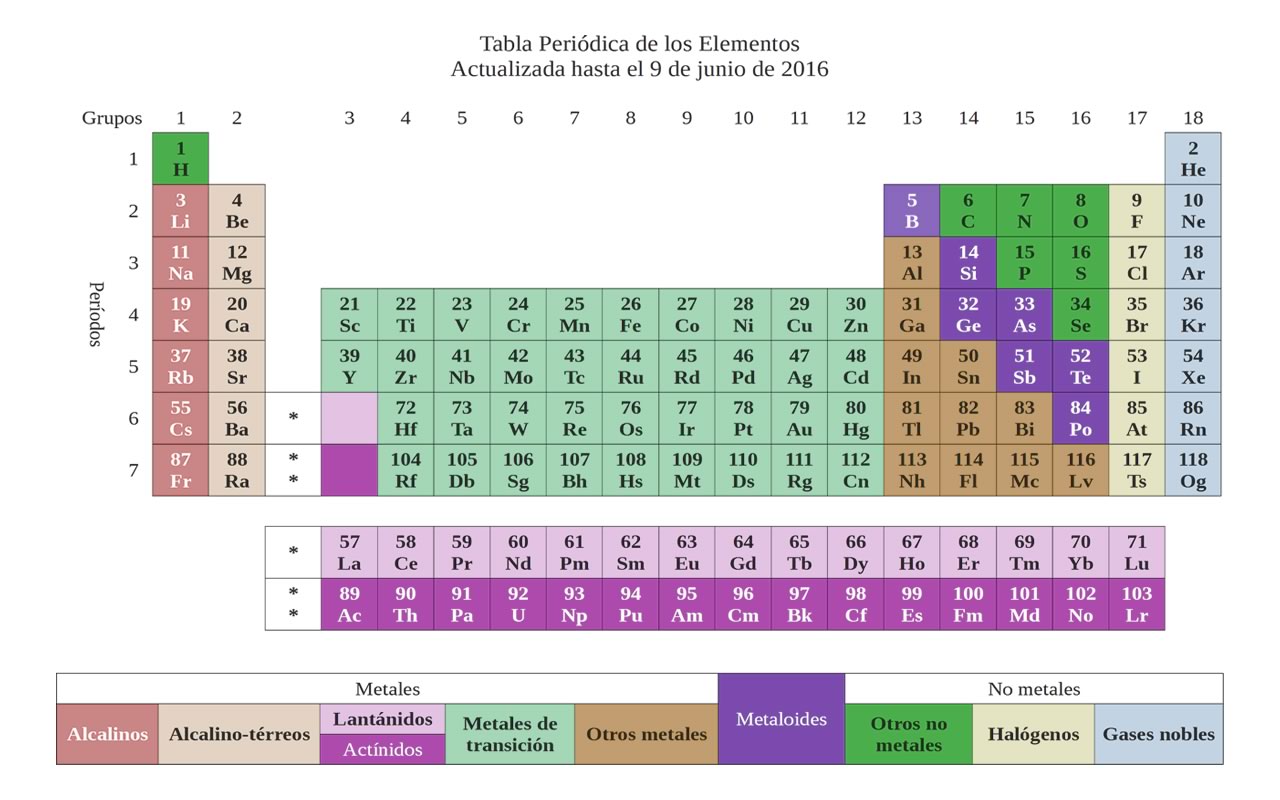
La tabla periódica
Este tema trata del arreglo u organización de los elementos en la tabla periódica y las principales características, usos e interpretaciones de la misma.
La organización de los elementos químicos en la tabla periódica ha sido uno de los logros más grandes de la humanidad en el conocimiento de la naturaleza, ya que permitió entender las propiedades y características de los elementos de manera organizada y realizar aplicaciones de éstos que en la naturaleza no se dan de manera espontánea. Muchos de los materiales de uso cotidiano se fabricaron gracias al conocimiento de las propiedades de las sustancias y elementos constituyentes.
Hubo varios intentos de organización de los elementos, pero fue Mendeléiev quien finalmente logró un arreglo consistente, que no dejaba ningún elemento conocido fuera del arreglo y a partir de allí incluso se propuso la existencia de elementos hasta ese momento desconocidos, con sus valores aproximados de peso atómico y propiedades. Más tarde se encontraron los elementos faltantes y se corroboró que coincidían con las predicciones de Mendeléiev. La base del arreglo de la tabla periódica de Mendeléiev fue el peso atómico y su organización en orden ascendente.
En 1914 otro químico, Henry Moseley, propuso el ordenamiento de los elementos de la tabla periódica no por su aumento en el peso atómico, sino por el aumento de su número atómico. Con este aporte quedó configurado el orden de los elementos tal como lo conocemos en la actualidad.
La tabla periódica
Ley periódica
En cuanto a las características y propiedades periódicas de los elementos, existen algunos puntos fundamentales que precisan el porqué de dicho arreglo. A continuación se presenta el punto más importante: Los elementos ordenados por sus números atómicos, presentan una evidente periodicidad en sus propiedades.
Como consecuencia de este enunciado se tiene que las propiedades físicas y químicas de los elementos (y en consecuencia de los compuestos constituidos por estos) se encuentran en dependencia periódica de sus números atómicos. Esto explica la importancia de entender el orden de los elementos en la tabla periódica para conocer sus propiedades y posibilidades de formar compuestos.
Los grupos químicos de elementos de la tabla periódica los constituyen las columnas de elementos que básicamente tienen semejanza en las propiedades químicas. Algunos de estos grupos de elementos tienen nombres especiales como metales alcalinos, metales alcalinotérreos, halógenos o gases nobles. Los grupos químicos de elementos en la tabla periódica, se tratarán en el siguiente tema.
La tabla periódica
Metales, metaloides (semimetales) y no metales
Otro punto importante sobre el arreglo de la tabla periódica es la siguiente clasificación:
- Elementos metálicos o metales, los cuales se clasifican a su vez en alcalinos y alcalinotérreos.
- Metaloides o semimetales.
- No metales, los cuales se clasifican en halógenos y gases nobles.
A continuación en la siguiente interactividad se encuentran las propiedades de cada uno.
La tabla periódica
Radio atómico
Con respecto a la ley periódica, una consecuencia es que los elementos (átomos) varían periódicamente en sus propiedades. Es decir, las propiedades de los elementos presentan cierta regularidad a lo largo de los grupos (columnas) y los periodos (filas) y a continuación revisaremos algunas de estas propiedades.
La primera propiedad periódica a revisar es el radio atómico. A continuación se presentan los valores del radio atómico de los elementos.
La tabla periódica
Potencial o energía de ionización
La segunda propiedad periódica que se revisara es el potencial o energía de ionización. El potencial de ionización es el valor de energía necesaria para remover el electrón menos unido al átomo, cuando éste se encuentra en estado gaseoso y está aislado y se forma un ion 1+ (catión).
Experimentalmente se calcula el valor del potencial de ionización por mol de electrones removidos. Por ejemplo, para el hidrógeno el potencial de ionización es 1312 kJ/mol. Se requieren 1312 kJ para remover un mol de electrones en un mol de átomos, un electrón por átomo.
Existen varios potenciales de ionización. El primero para remover el primer electrón del átomo. El segundo potencial de ionización para remover el segundo electrón del átomo, después de haber removido el primero; y el tercer potencial de ionización es la energía necesaria para remover el tercer electrón, una vez removidos los dos primeros electrones del átomo. Remover más electrones es difícil por la atracción que experimentan los electrones remanentes por el núcleo. El orden del valor de potencial de ionización es el siguiente: PI3 > PI2 > PI1. Remover un electrón adicional en un átomo, cada vez requiere mayor energía. Revisemos el siguiente ejemplo del calcio, como apliación temática.
La tabla periódica
Afinidad electrónica
La tercera propiedad periódica a revisar es la afinidad electrónica. La afinidad electrónica es el valor de energía que absorbe o expulsa un átomo en estado gaseoso y aislado, cuando se le adiciona un electrón para formar un ión 1- (anión). Experimentalmente se calcula el valor de la afinidad electrónica por mol de electrones adicionados. Veamos los siguientes ejemplos, como ampliación temática.
A los procesos que liberan energía se les denomina exotérmicos y el valor de la energía aparece en los productos, porque aparece el exceso de energía al final de la reacción. Con la configuración electrónica se puede revisar si el proceso es endotérmico (no favorable) o exotérmico (favorable). Los elementos con configuración electrónica que cierre periodo, subnivel o semi-llene subnivel no será favorable el proceso de adición de electrones porque tienen configuración electrónica estable.
La tabla periódica
Electronegatividad
La cuarta propiedad periódica a revisar es la electronegatividad, la cual es una medida relativa de la tendencia de un átomo a atraer o ganar los electrones cuando forma un enlace con otro átomo.
Los elementos con mayor electronegatividad (no metales) ganan los electrones del enlace y los menos electronegativos (metales) los pierden. Los elementos que ganan electrones forman aniones (iones negativos) y los que los pierden cationes (iones positivos).
 |
Si colocamos en orden ascendente de electronegatividad al B, Na, F y O, encontramos que: Na < B < O < F. Por lo tanto, el fluor le gana los electrones del enlace al Na, B y C. El oxígeno le gana los electrones del enlace al Na y B. Finalmente el boro le gana los electrones al sodio. De esta manera, se interpreta la electronegatividad. |
La tabla periódica
Números de oxidación
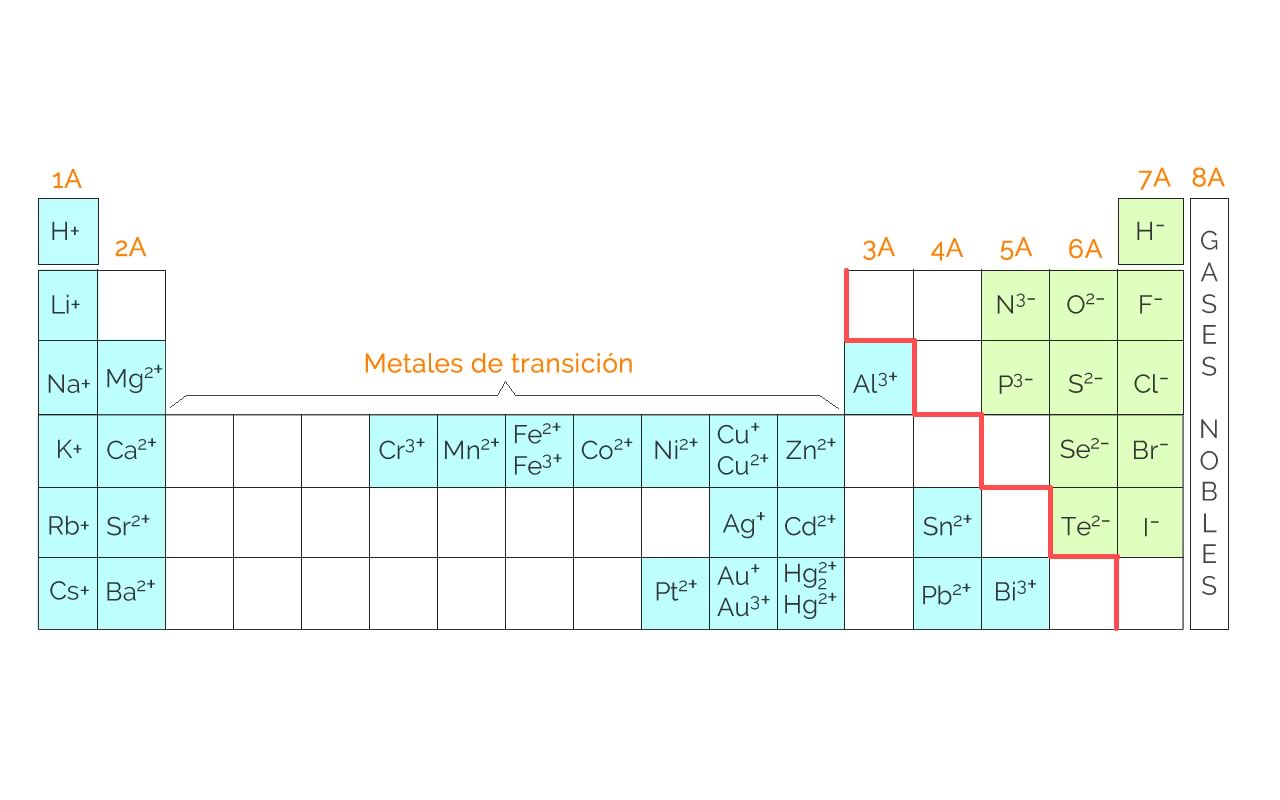
Finalmente se revisarán los números de oxidación de los elementos. El número de oxidación es el valor de la carga eléctrica que adquiere un átomo o elemento cuando forma una molécula o compuesto.
El elemento más electronegativo del compuesto gana los electrones y adquiere carga o número de oxidación negativo. Los demás elementos adquieren número de oxidación positivo en la molécula. Los números de oxidación se obtienen revisando cuantos electrones gana o pierde el elemento para adquirir configuración de gas noble o estable.
Lo primero que se revisa es el elemento más electronegativo del compuesto y luego los demás. Veámoslo en la ampliación temática con el siguiente ejemplo: ácido sulfúrico, H2SO4.
Actividad de aprendizaje
 |
Contesta falso o verdadero a los enunciados formulados sobre la tabla periódica y sus propiedades. |
Resumen
Esta unidad está dedicada a presentar los conceptos y características principales de los átomos, constituyentes mínimos de los elementos.
Se comienza con una presentación de los principales modelos atómicos desarrollados en el siglo XIX, se revisa la visión moderna de la estructura del átomo o modelo cuántico del átomo, que da las bases para explicar las propiedades de los elementos y su reactividad, y se finaliza con la revisión de las propiedades periódicas de los elementos que son la base fundamental para explicar la capacidad de los elementos para formar enlaces químicos.
Bibliografía ()
- Acosta, G. (2010) Manual de Laboratorio de Química General (2da Ed). Bogotá: Universidad Militar Nueva Granada.
- Briceño, C. Y Rodríguez, L. (1993) Química Bogotá: Editorial Educativa, UIS.
- Brown, T. Lemay,H. y Bursten (2009) Química, la ciencia central (11vª Ed) México: Prentice Hall.
- Chang, R. (2010) Química (10ma Ed) México: Ed. Mc Graw-Hill
- Corporación Autónoma Regional de Cundinamarca – CAR (2010) Adecuación hídrica y recuperación ambiental del rio Bogotá. Vol I y II. Bogotá D.C.: Corporación Autónoma Regional de Cundinamarca – CAR.
- Drew, W. (1990). Química general orgánica y biológica. Bogotá, Colombia: McGraw-Hill Latinoamericana S.A.
- Fred, R. (1992) Fundamentos de química. México: Prentice-Hall Hispanoamericana s.a.,
- Hein, M., Arena, S. (2005) Fundamentos de química, (11va Ed) MéxicoD.F.: Thomson Editores, S.A.
- Kotz, J.C. y Treichel, P.M. (2003) Química y reactividad química. (5ta Ed) México D.F.: Thomson.
- MERCK COLOMBIA S.A (1995) El a, b, c, de la seguridad en el laboratorio (3ra Ed). Bogotá, Colombia: Departamento L PRO.
- Mortimer, C. (1985) Química Belmont California. U.S.A: Grupo Editorial Ibero América.
- Peck, L. (1980) Journal of Chemical Education. 57 (517)
- Petrucci, R. (1986) Química General. México: Fondo Educativo Interamericano.
- Routh, J. Eyman, D., Burton, D. (1900) Compendio esencial de química general orgánica y bioquímica. Bogotá, Colombia: Editorial Reverté Colombiana, s.a.
- Rusell, J., Larena, A. (1992) Química General. Bogotá, Colombia: McGraw-Hill Latinoam. S.A.
- Umland, J.B. y Bellama, J.M. (2000) Química General. (3ra Ed) México D.F.: Thomson.
- Vega, J.C. (1992) Química Orgánica para estudiantes de Ingeniería. Santiago: Universidad Católica de Chile
- Whitten, D., Peck, S. (2008) Química (8va Ed) HITTEN, México: Cengage Learning, 2008, Cruz Manca, México
- Wittcott, H., Reuben, B. (1997) Productos químicos orgánicos industriales, I y II, México: Editorial Limusa
Referencias Web
- Quevedo, J. (s.f.) Alfonso Formula (s.f.) Formulación de química inorgánica. [online] Alonsoformula.com.https://www.alonsoformula.com/inorganica/
- ThoughtCo. (s.f.). Famous Chemists and their Achievements. [online]https://www.thoughtco.com/famous-chemists-4133583
- ThoughtCo. (s.f.). Chemistry in Everyday Life. [online]https://www.thoughtco.com/chemistry-in-everyday-life-4133585
- YouTube. (s.f.). SOLOCONOCIMIENTO [online]https://www.youtube.com/user/soloconocimiento
- WebElements. The perodic table of the elements. WebElements.https://www.webelements.com/