Introducción
La necesidad del hombre por generar una manera de conocer su entorno, ha motivado la búsqueda de una forma de indicar el estado en el que se encuentra un sistema; la cual sea comprensible por los demás, reproducible y atinente con la verdad para ser aceptada por la comunidad. De acuerdo con esto, se llegó en algunos casos a acuerdos en conceptos que posteriormente fueron rechazados por evidencias contrarias.
La unidad patrón para las características que se pueden determinar es ejemplo de ello, puesto que con la “unificación” de los patrones se logró transmitir en forma confiable la información. Aunque no pudo ser internacional, ya que países como Inglaterra y Estados Unidos conservaron el sistema de medida tradicional para ellos.
Ahora bien, continuando con la unidad de patrón, al reportar un dato de medida se debe tener en cuenta la fineza del instrumento utilizado para tal fin y se ve reflejado en la cantidad de cifras significativas y las operaciones con las mismas.
Las características que presentan las sustancias a condiciones normales de presión y temperatura nos permiten clasificar en tres estados fundamentales, a saber: sólido, líquido y gaseoso. Las sustancias puras al estar contaminadas con otras, sin que exista reacción entre las mismas, reciben el nombre de mezclas. Para poder realizar medidas de conteo de partículas en el laboratorio se hace necesario una gran cantidad de ellas por consiguiente se usa la cantidad mol, consistente en 6,022x1023 unidades, también conocido como número de Avogadro en honor a Amadeo Avogadro.
Objetivos
Objetivo general
Dar las herramientas necesarias para realizar la toma de datos, conversión y operaciones entre los mismos con el fin de establecer relaciones entre el hombre y su entorno.
Objetivos específicos
- Clasificar las sustancias según el estado de agregación.
- Conocer las unidades fundamentales y derivadas para los sistemas de medida.
- Hacer los cambios entre unidades dentro de los sistemas y entre ellos.
- Tomar datos experimentales con la cantidad adecuada de cifras significativas.
- Realizar operaciones entre valores experimentales, teniendo en cuenta las reglas para cifras significativas.
- Distinguir entre precisión y exactitud, aplicando los conceptos a datos experimentales.
- Conocer las etapas del método científico.
Materia y estados de agregación o fases. Elementos, ecompuestos y mezclas
La materia entendida como todo aquello que ocupa un lugar en el espacio, con las propiedades de masa y volumen, da los parámetros para enmarcar un sistema dentro de los alrededores, lo inmaterial no tiene fronteras definidas que permitan delimitarlo inequívocamente. La clasificación de las sustancia según su estado de agregación permite determinar el comportamiento del sistema y por ende las propiedades.
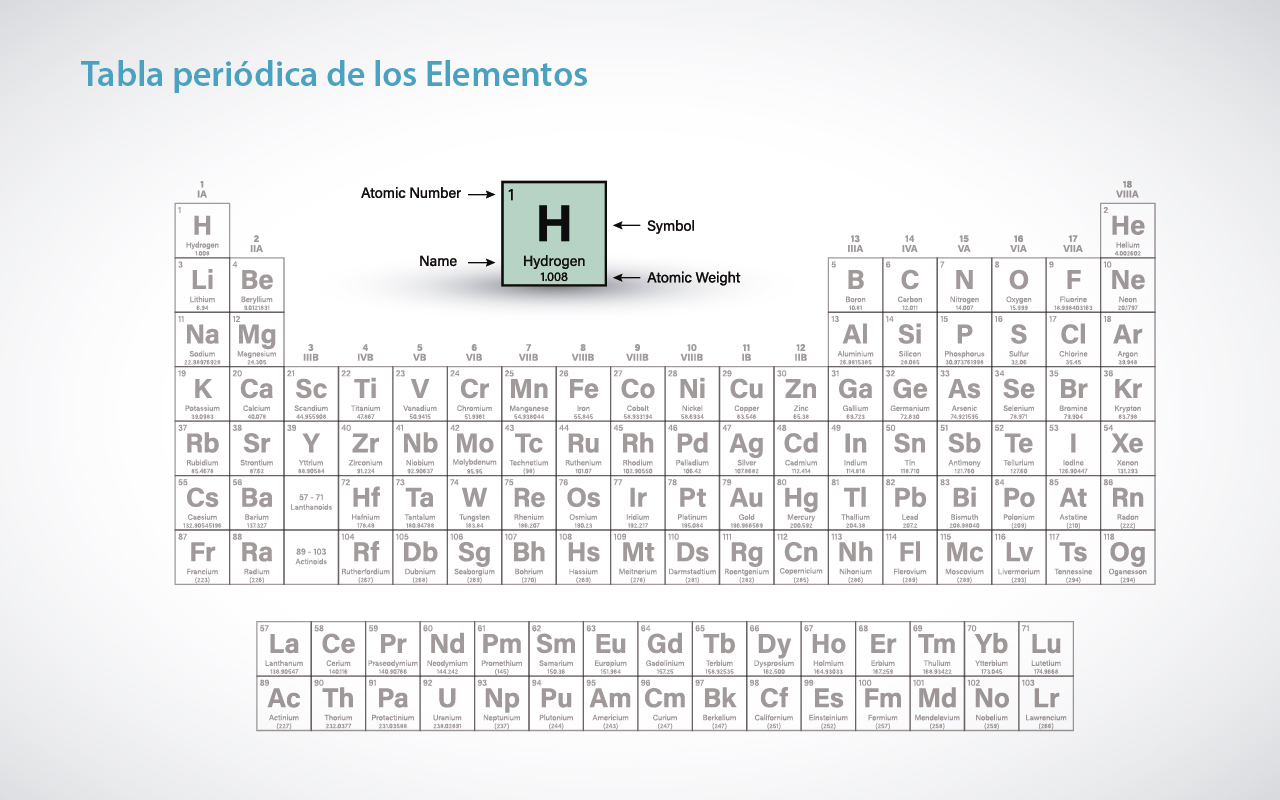
Los elementos como piezas básicas de la formación de todas las sustancias conocidas en el universo son limitadas, pero la gran posibilidad de combinaciones es lo que hace de la química un área del conocimiento tan amplia con enormes posibilidades de desarrollo e investigación.
Cuando dos sustancia se unen sin que entre ellas exista reacción química se dice que se forma una mezcla, en la cual cada una de las sustancia conserva sus propiedades y no se forma ni destruyen enlaces. Las mezclas pueden ser separadas en sus constituyentes con el uso de métodos físicos de separación, como por ejemplo el tamizado, la destilación, la decantación entre otros.
Materia y estados de agregación o fases. Elementos, ecompuestos y mezclas
¿Qué es materia? estados de agregación y diagrama de fases
Como se dijo antes, se considera como materia a todo aquello que ocupa un lugar en el espacio. Los estados de agregación más comunes son el sólido, líquido y gaseoso. No todas las sustancias pueden tenerse en estos tres estados, es así como algunas se descomponen por debajo de su punto de fusión o de ebullición a condiciones normales de presión.
- Sustancias en estado sólido: poseen forma y volumen constantes, y a nivel microscópico podemos afirmar que las partículas que las constituyen se encuentran en sitios fijos unas respectos a las otras.
- Sustancias en estado líquido: tienen volumen constante y toman la forma de la parte inferior del recipiente que los contiene, si nos referimos a las partículas constituyentes, se puede afirmar que entre ellas existe atracción mediana que les permite cambiar la forma sin cambiar el volumen.
- Sustancias en estado gaseoso: en este grupo se considera que no tienen volumen ni forma constante, ya que ocupa todo el recipiente que lo contiene y toma la forma del mismo.
 |
Para complementar la anterior información, se recomienda visualizar el siguiente video |
Materia y estados de agregación o fases. Elementos, ecompuestos y mezclas
Elementos compuestos y mezclas
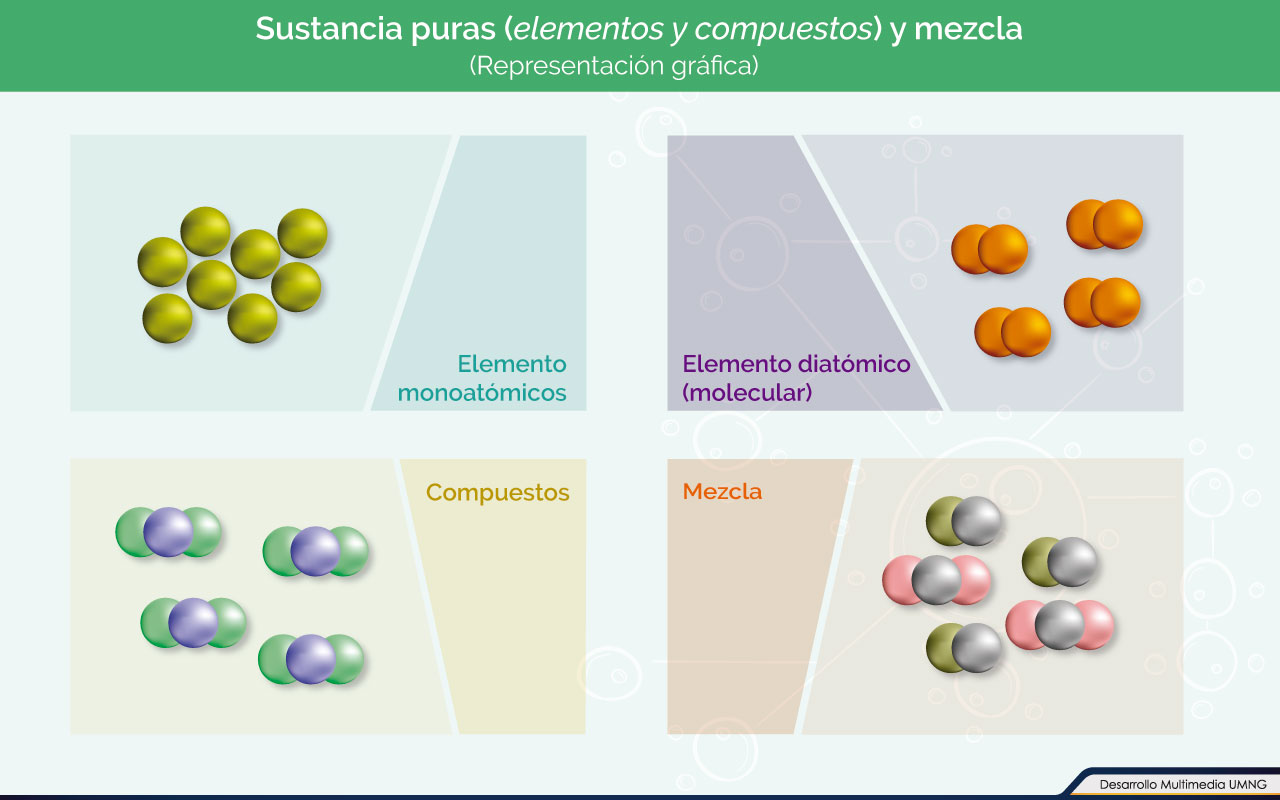
Al referirnos a sustancia puras, se entiende que son aquellas sustancia que están constituidas por una sola clase de unidades básicas, es decir por solo un tipo de elemento o compuesto.
Los elementos son todas aquellas sustancias constituidas por una misma especie de átomos y que no se pueden descomponer en sustancias más elementales. Los compuestos, por su parte, también son sustancias, pero en este caso se puede descomponer en sustancias más simples.
Las mezclas se pueden clasificar en dos grandes grupos: homogéneas y heterogéneas.
Las homogéneas son aquellas donde la compatibilidad de las sustancias que en ella intervienen hacen que se cree un medio en el cual no se puede distinguir donde se encuentra cada una. En las heterogéneas, por su parte, sí es posible diferenciar las propiedades en el medio a medida que nos desplazamos en el recipiente.
 |
Como ejemplo de lo anterior, se recomienda ver cómo se hacen los perfumes. |
Medidas, sistemas de unidades, conversiones de valores y cifras significativas
Medir es comparar una característica del sistema estudiado contra un patrón de medida, estableciendo la relación en forma cuantitativa. Para medir se debe conocer cuál es la propiedad a medir y si existe o no un patrón de comparación.
La objetividad en la medida es el pilar fundamental para establecer los valores a reportar. Algunas cualidades de los sistemas no son cuantificables debido a la inexistencia de un patrón de comparación.
Medidas, sistemas de unidades, conversiones de valores y cifras significativas
Método científico
Dentro del acercamiento a la naturaleza, el hombre ha generado un grupo de pasos a seguir, que sin ser camisa de fuerza permite generar un orden empírico que puede mostrar un camino para llegar a una proximidad de la realidad.
Los pasos resumidos son:
- Toma de datos.
- Planteamiento de una hipótesis como explicación tentativa de los datos anteriormente recolectados.
- Comprobación de la hipótesis en forma experimental, que permite determinar la veracidad o negación de la hipótesis en forma inequívoca.
- Rectificación de la hipótesis.
Medidas, sistemas de unidades, conversiones de valores y cifras significativas
Medida, precisión, exactitud y error
En el primer paso del método científico se desea realizar una toma de datos del sistema que está siendo sometido a estudio. Para ello es necesario realizar una comparación del atributo del sistema contra el patrón de la misma propiedad, que permita determinar en la forma más objetiva posible el valor real.
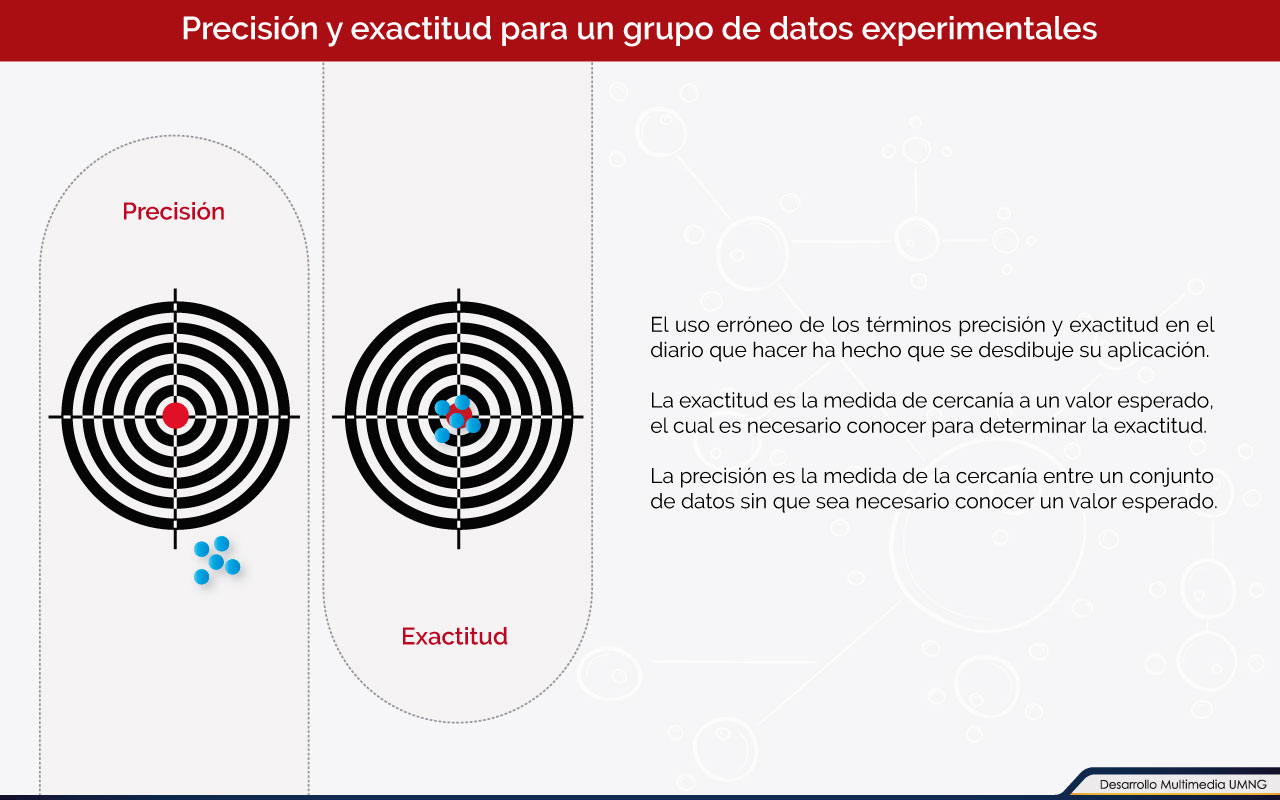
En caso de conocer el valor real de una medida y comparar contra un valor experimental se puede determinar la exactitud de la medida, aduciendo a la cercanía o proximidad del valor esperado y el valor real o teórico.
Al realizar en varias oportunidades la misma medida puede que se presenten dispersos o alejados unos de otros, en este caso podemos decir que no hay precisión, contrario a lo anterior cuando un grupo de datos tomados para una misma medida están cercanos unos de otros, es decir poco dispersos; entonces se habla de que hay precisión en ese conjunto de datos. Como símil se puede considerar el juego del tiro al blanco en donde quien esté cerca del centro de los círculos concéntricos se le considera con gran precisión.
Cuando se conoce el valor teórico o esperado y tenemos un valor experimental podemos determinar el error que se cometió, el cual se explica en la anterior ampliación temática.
Medidas, sistemas de unidades, conversiones de valores y cifras significativas
Cifras significativas y notación científica
Al tomar una medida se tiene certeza de algunos de los números reportados, la cantidad de éstos depende del instrumento usado para realizar la determinación, pero la última de las cifras reportadas depende del observador y por ende, es una cifra dudosa. La cantidad de cifras reportadas consta de una parte certera y una parte dudosa, así es que el conjunto total constituyen las cifras significativas para esta medida.
Luego de tomar medidas se operan entre sí para obtener nuevos resultados, es allí donde surge la pregunta de con cuántas cifras significativas debe ser reportado el resultado. Para contestar, se deben seguir las normas en el resultado que indica que, cuando se realiza una suma o una resta se deben conservar la cantidad de cifras decimales que posea el que menos cantidad de éstas tenga. En el caso de realizar una multiplicación o división, el resultado será reportado con la cantidad de cifras significativas del menor de los factores que en ella interviene.
Cuando se reportan datos en notación científica se debe dejar una cifra correspondiente a los enteros y el resto estará en los decimales; para el fin antes mencionado se puede hacer necesario cambiar la posición en la que se encuentra el símbolo que los separa. Esto debe ser compensado multiplicando por el factor adecuado consistente en potencias de 10. A continuación se explica a detalle esta notación científica.
Medidas, sistemas de unidades, conversiones de valores y cifras significativas
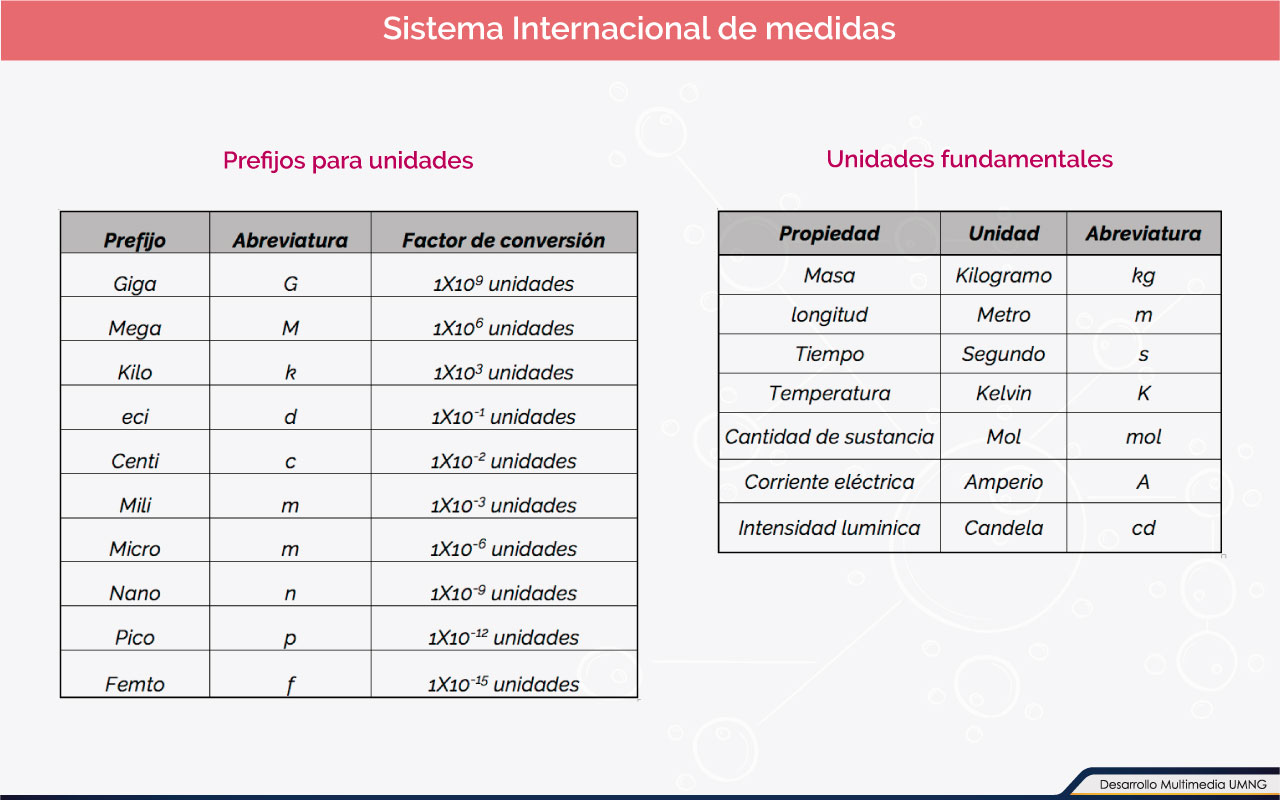
Sistema de unidades y factores de conversión
Las unidades fundamentales deben tener un patrón de medida para cada una de ellas. A nivel internacional se tiene el sistema de unidades para longitud (metro), tiempo (segundo), masa (kilogramo), cantidad de corriente eléctrica (amperios), luminosidad (candela), temperatura (grados kelvin) y cantidad de materia (mol).
Para describir un objeto es necesario medir sus características, entre ellas se encuentran las que no pueden ser expresadas en términos de otras. Por ejemplo, ante la pregunta ¿qué hora es?, la respuesta no puede ser dada en metros (longitud) pues sería incoherente. Estas unidades que no se pueden expresar en términos de otras se le conoce como unidad fundamental. Las unidades que se expresa en términos de otras se conocen como unidades derivadas.
Pero existen atributos de los sistemas que no son medibles ya que no existe un patrón de comparación y su valor depende del observador.
Las propiedades se pueden clasificar en dos grandes grupos dependiendo de su comportamiento como variable o constante a medida que varía el tamaño de la muestra. Cuando una propiedad permanece constante sin importar el tamaño de la muestra se dice que esa propiedad es intensiva y cuando no permanece constante cuando cambia el tamaño se dice que la propiedad es extensiva.
Pesos atómicos y moleculares
Al establecer una forma de medir los átomos se consideró una comparación entre ellos en donde el más pequeño fuera la unidad básica. Es decir que el valor para el peso del ya mencionado correspondiera a la unidad, determinada como unidad de masa atómica (uma). Cada uno de los demás se expresan en función de este.
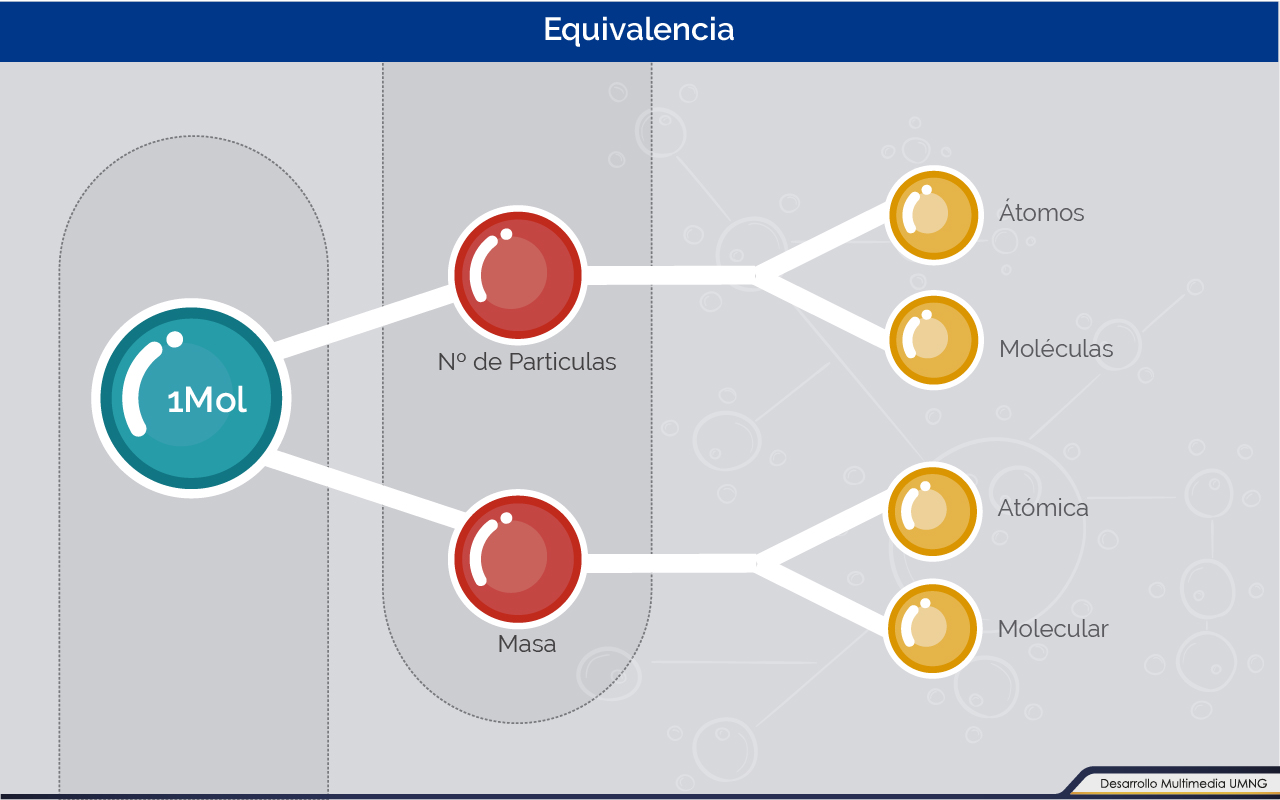
Debido a la imposibilidad de pesar un solo átomo se debe hacer uso de grandes cantidades de estos para poder realizar una medida empírica. Cuando se habla de una decena se sabe que se refiere a diez unidades, al decir docena imaginamos doce unidades, al manifestar una centena consideramos cien unidades, si tenemos una resma se conoce que son 500 unidades y cuando se refieren a una mol son 6,022X1023 unidades.
La gran contribución de la cantidad conocida como mol es que si los pesos atómicos de los elementos se expresan en gramos y no en umas, en esa cantidad tendremos un mol de ese elemento. Recuerde que mol es una cantidad de unidades.
Pesos atómicos y moleculares
Fórmula empírica y molecular
La fórmula empírica para una sustancia muestra la relación o proporción mínima en la cual se encuentran los componentes, en números enteros mediante subíndices.
La fórmula molecular indica el número o cantidad de átomos de cada elemento que forman una molécula para la sustancia pura, conservando la relación dada por la fórmula empírica. Es decir, que los subíndices de la fórmula molecular son fruto de los subíndices de la fórmula empírica multiplicados por un número entero dentro de los que se considera el uno. Con lo último se puede inferir que puede ocurrir que la fórmula empírica sea la misma fórmula molecular. Es necesario conocer el peso molar de la sustancia para poder determinar la fórmula molecular, ya que de no conocerlo se tiene un grupo infinito de combinaciones de átomos que cumple la proporción.
Para determinar la fórmula empírica se lleva cada uno de los elementos constituyentes a moles y en esa condición se dividen las moles de cada elemento entre el menor valor para el grupo. En caso de que no todos generen números enteros, o muy cercanos a un entero, se procede a multiplicar por valores enteros cada vez mayores comenzando por el dos hasta que se llegue a valores enteros o muy cercanos a ellos. Recuerde que cuando se multiplica para buscar un entero debe multiplicar a todos por el mismo entero. Los valores enteros obtenidos corresponden a los subíndices para cada elemento en la fórmula empírica.
La formula molecular está relacionada con la fórmula empírica de forma que el peso de la fórmula molecular es múltiplo de la fórmula empírica. Es decir que el peso de la fórmula molecular es el peso de fórmula empírica multiplicado por un entero, de igual forma los subíndices de la fórmula molecular son múltiplos de los subíndices de la fórmula empírica, sin descartar que el entero por el que ha de multiplicarse la fórmula empírica sea uno, lo que implica que la fórmula molecular sea igual a la empírica.
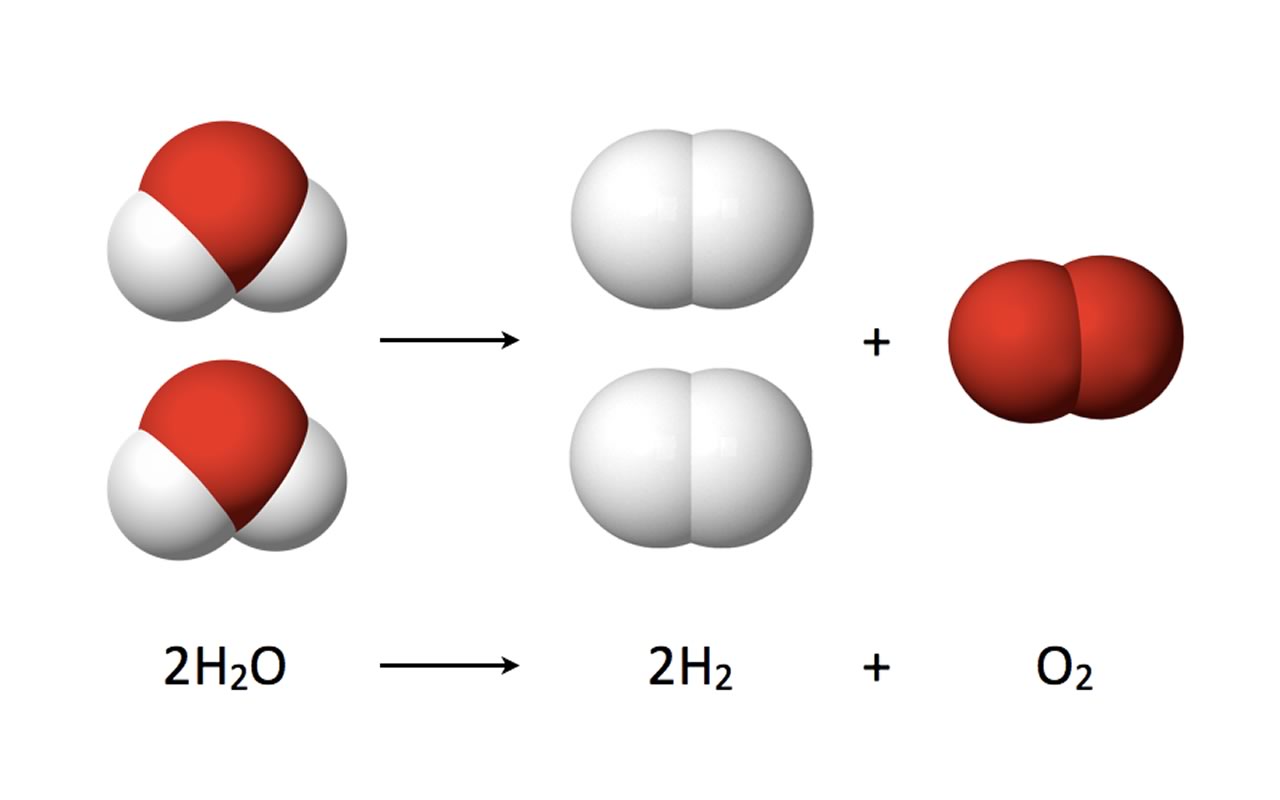
Cambios físicos y químicos de la materia, propiedades
Cuando tenemos en un proceso la formación o ruptura de enlaces se dice que ocurre una reacción química, los demás procesos son cambios físicos. Se debe evitar confundir los cambios físicos con las propiedades físicas.
Pues los cambios son modificaciones del sistema, mientras que las propiedades son los atributos del sistema en un instante dado.
Cantidad de sustancia, el mol y el número de Avogadro
Al solicitar que un alumno realice el conteo de 1000 (1x103) elementos en el laboratorio implicaría una labor extensa y cuando se requiere contar 1 000 000 000 (1x109) elementos sería una labor muy demorada, más allá de estos valores se encuentra 6,022x1023 (cercano a medio cuatrillón) y que no se tiene la posibilidad de contabilizarlo aunque dedicáramos la vida entera en esta labor. Para poder contar cantidades de unidades tan grandes se optó por usar el mol y su relación con la masa atómica de los elementos.
Como ya se manifestó con anterioridad al nombrar “mol” se debe entender como una cantidad de unidades, correspondiente a 6,022x1023 unidades. Este número se conoce también como número de Avogadro en honor a Amadeo Avogadro. Podemos tener un mol de átomos, un mol de moléculas, un mol de sillas, un mol de esferos, y en todos los casos se refiere a una cantidad de unidades. Al realizar cálculos para determinar el reactivo limitantes se tiene la posibilidad de realizarlos mediante la relación de los reactivos en moles.
Actividad de aprendizaje

|
Repasa y fortalece los conceptos de esta unidad con la siguiente actividad. |
Resumen
Con el fin de recopilar datos del entorno se requiere medir, dando una comparación entre el patrón de medida y la propiedad de sistema en estudio. La recolección de datos, que se debe ajustar a un sistema de medidas, es el primer paso dentro del método científico. Para los datos recolectados se puede determinar su precisión y exactitud. Posteriormente en el método científico se postula una hipótesis para explicar los datos tomados, esta hipótesis deberá ser comprobada y en caso necesario corregida.
Las sustancias se pueden clasificar como puras o mezclas. Las sustancias puras se dividen en elementos y compuestos, dependiendo si se encuentran constituidas por una clase o más de átomos, respectivamente.
Bibliografía ()
- Acosta, G. (2010) Manual de Laboratorio de Química General (2da Ed). Bogotá: Universidad Militar Nueva Granada.
- Briceño, C. Y Rodríguez, L. (1993) Química Bogotá: Editorial Educativa, UIS.
- Brown, T. Lemay,H. y Bursten (2009) Química, la ciencia central (11vª Ed) México: Prentice Hall.
- Chang, R. (2010) Química (10ma Ed) México: Ed. Mc Graw-Hill
- Corporación Autónoma Regional de Cundinamarca – CAR (2010) Adecuación hídrica y recuperación ambiental del rio Bogotá. Vol I y II. Bogotá D.C.: Corporación Autónoma Regional de Cundinamarca – CAR.
- Drew, W. (1990). Química general orgánica y biológica. Bogotá, Colombia: McGraw-Hill Latinoamericana S.A.
- Fred, R. (1992) Fundamentos de química. México: Prentice-Hall Hispanoamericana s.a.,
- Hein, M., Arena, S. (2005) Fundamentos de química, (11va Ed) MéxicoD.F.: Thomson Editores, S.A.
- Kotz, J.C. y Treichel, P.M. (2003) Química y reactividad química. (5ta Ed) México D.F.: Thomson.
- MERCK COLOMBIA S.A (1995) El a, b, c, de la seguridad en el laboratorio (3ra Ed). Bogotá, Colombia: Departamento L PRO.
- Mortimer, C. (1985) Química Belmont California. U.S.A: Grupo Editorial Ibero América.
- Peck, L. (1980) Journal of Chemical Education. 57 (517)
- Petrucci, R. (1986) Química General. México: Fondo Educativo Interamericano.
- Routh, J. Eyman, D., Burton, D. (1900) Compendio esencial de química general orgánica y bioquímica. Bogotá, Colombia: Editorial Reverté Colombiana, s.a.
- Rusell, J., Larena, A. (1992) Química General. Bogotá, Colombia: McGraw-Hill Latinoam. S.A.
- Umland, J.B. y Bellama, J.M. (2000) Química General. (3ra Ed) México D.F.: Thomson.
- Vega, J.C. (1992) Química Orgánica para estudiantes de Ingeniería. Santiago: Universidad Católica de Chile
- Whitten, D., Peck, S. (2008) Química (8va Ed) HITTEN, México: Cengage Learning, 2008, Cruz Manca, México
- Wittcott, H., Reuben, B. (1997) Productos químicos orgánicos industriales, I y II, México: Editorial Limusa
Referencias Web
- Amigos de la Química. (5 de marzo de 2018). QUÍMICA ¿Qué es un MOL?. [Video]. Recuperado de: https://www.youtube.com/watch?v=FrfRSiDGVjA.
- Quevedo, J. (s.f.) Alfonso Formula (s.f.) Formulación de química inorgánica. [online] Alonsoformula.com.https://www.alonsoformula.com/inorganica/
- ThoughtCo. (s.f.). Famous Chemists and their Achievements. [online]https://www.thoughtco.com/famous-chemists-4133583
- ThoughtCo. (s.f.). Chemistry in Everyday Life. [online]https://www.thoughtco.com/chemistry-in-everyday-life-4133585
- YouTube. (s.f.). SOLOCONOCIMIENTO [online]https://www.youtube.com/user/soloconocimiento
- WebElements. The perodic table of the elements. WebElements.https://www.webelements.com/